
| �¶� n��CO�� ʱ�� | 0 | 10 | 20 | �� | 40 | 50 |
| T1 | 1.0 | 0.7 | 0.5 | �� | 0.25 | 0.25 |
| T2 | 1.0 | 0.65 | 0.4 | �� | 0.28 | 0.28 |
| A�� | T1�¶���ƽ�������ٳ���0.5molCO������ƽ���CO�ܵ�ת������H2��� | |
| B�� | T1�¶���10-20sH2�ķ�Ӧ����Ϊ0.04mol•L-1•s-1 | |
| C�� | �÷�Ӧ�ġ�����0 | |
| D�� | T2�¶���ƽ���㶨ѹǿ�������0.28molCH3OH��CH3OH������������� |
���� A��ƽ�������ٳ���0.5molCO����pV=nRT��֪��n����ѹǿ����ƽ�������ƶ�������ʼ��֮�ȵ��ڻ�ѧ������֮��ʱ��ת������ͬ��
B�����v=$\frac{��c}{��t}$���㣻
C���ɱ������ݿ�֪��T2�ķ�Ӧ���ʴ���ƽ��ʱCO�ĺ�����
D��ƽ���㶨ѹǿ�������0.28molCH3OH����pV=nRT��֪��n����V������ѹǿ��С��ƽ�������ƶ���
��� �⣺A��ƽ�������ٳ���0.5molCO����pV=nRT��֪��n����ѹǿ����ƽ�������ƶ�����ЧΪ
CO��g��+2H2��g��?CH3OH��g��
��ʼ 0.75 1.5 0
ת�� x 2x x
CO����������ʼ��֮�ȵ��ڻ�ѧ������֮�ȣ�$\frac{x}{0.75}$=$\frac{2x}{1.5}$��������ƽ���CO�ܵ�ת������H2��ȣ���A��ȷ��
B��T1�¶���10-20sCO�ķ�Ӧ����Ϊ$\frac{\frac{0.3mol}{2L}}{10s}$=0.015mol•L-1•s-1��������֮�ȵ��ڻ�ѧ������֮�ȿ�֪��10-20sH2�ķ�Ӧ����Ϊ0.03mol•L-1•s-1����B����
C���ɱ������ݿ�֪��T2�ķ�Ӧ���ʴ���ƽ��ʱCO�ĺ������������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ����C����
D��ƽ���㶨ѹǿ�������0.28molCH3OH����pV=nRT��֪��n����V������ѹǿ��С��ƽ�������ƶ�����CH3OH�����������С����D����
��ѡA��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ�߿��������ͺ�Ƶ���㣬����ת���ʵļ��㡢���ʼ��㡢ƽ���ƶ�Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��������ݵ�Ӧ�ã���Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɱ������ | B�� | ʹˮ�д�����ֽ� | ||
| C�� | ���ˮ���¶� | D�� | ����ˮ�������ĺ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 14g��ϩ�ͱ�ϩ��������е���ԭ����Ϊ2NA | |
| B�� | 7.8g Na2S�����7.8g Na2O2�����к��е���������Ŀ��Ϊ0.1NA | |
| C�� | ��״���£�5.6L������̼�����к��е���ԭ����ĿΪ0.5NA | |
| D�� | 0.5mol/LHCl ��Һ�к��е���������Ϊ0.05NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | W��Y����������ﶼ������ | |
| B�� | Y��Z�γɵĻ�����һ��Ϊ���ۻ����� | |
| C�� | ����Ԫ����WԪ�صķǽ�������ǿ | |
| D�� | W��X��Y��Z��ԭ�Ӱ뾶��С˳��һ���ǣ�Z��Y��X��W |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ���� | 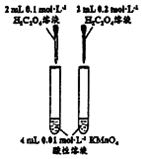 |  | 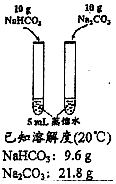 |  |
| Ŀ�� | ̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�� | �Ʊ����� | �����±Ƚ�NaHCO3��Na2CO3���ܽ�� | ̽���¶ȶԻ�ѧƽ���Ӱ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol I2��s����ͨ��2 g H2��g������Ӧ����26.48 kJ | |
| B�� | 1 mol��̬����1 mol��̬���������������17.00 kJ | |
| C�� | ��Ӧ�������ķ�Ӧ���������ȷ�Ӧ�������ķ�Ӧ���������� | |
| D�� | ��Ӧ�������ų��������࣬���Բ���������ͣ��ȷ�Ӧ�������IJ�����ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | lmol Na2O2������ˮ��Ӧ�����������������ת�Ƶĵ�����Ϊ2��6.02��1023 | |
| B�� | SiO2��s��+2C��s��=Si��s��+2CO��g���ڳ����²����Է����У���÷�Ӧ�ġ�H��0 | |
| C�� | ϡ��0.1 mol•L-1CH3COOH��Һ����Һ����������Ũ�Ⱦ���С | |
| D�� | Ǧ�����ڳ������У��������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
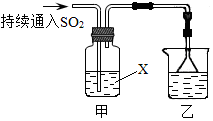
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com