

 ;
;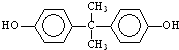 )在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:2n
)在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:2n +n
+n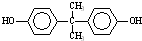 →
→ +4nCH3OH.
+4nCH3OH. 分析 由合成流程可知,反应①为加成反应生成环氧乙烷,反应②为C=O键的加成反应,反应③为C与甲醇的取代反应生成DMC( )和X(OHCH2CH2OH),然后结合有机物的结构与性质来解答.
)和X(OHCH2CH2OH),然后结合有机物的结构与性质来解答.
解答 解:由合成流程可知,反应①为加成反应生成环氧乙烷,反应②为C=O键的加成反应,反应③为C与甲醇的取代反应生成DMC( )和X(OHCH2CH2OH),
)和X(OHCH2CH2OH),
(1)由上述分析可知,①为加成反应,
故答案为:加成反应;
(2)由上述分析可知,X为OHCH2CH2OH,
故答案为:OHCH2CH2OH;
(3)Y与DMC互为同分异构体,Y的水溶液呈酸性,在一定条件下2mol Y能生成1mol分子中含六元环结构的有机物Z,Y中含1个-COOH,则Y的结构简式为CH3CH(OH)COOH,Z为 ,
,
故答案为: ;
;
(4)DMC与双酚( )在一定条件下可生成芳香族聚碳酸酯,反应的化学方程式为:2n
)在一定条件下可生成芳香族聚碳酸酯,反应的化学方程式为:2n +n
+n →
→ +4nCH3OH,
+4nCH3OH,
故答案为:2n +n
+n →
→ +4nCH3OH.
+4nCH3OH.
点评 本题考查有机物推断与合成、有机反应类型、同分异构体书写等,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,易错点为(4),注意理解给予信息.


科目:高中化学 来源: 题型:多选题
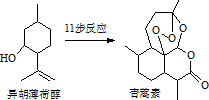 2015年我国药物化学家屠吆吆因发明抗疟疾新药青蒿素和双氢青蒿素被授予诺贝尔生理学或医学奖.以异胡薄荷醇为起始原料是人工合成青蒿素的途径之一(如图).下列说法正确的是( )
2015年我国药物化学家屠吆吆因发明抗疟疾新药青蒿素和双氢青蒿素被授予诺贝尔生理学或医学奖.以异胡薄荷醇为起始原料是人工合成青蒿素的途径之一(如图).下列说法正确的是( )| A. | 异胡薄荷醇遇FeCl3溶液显紫色 | |
| B. | 异胡薄荷醇可发生消去反应、加成反应 | |
| C. | 青蒿素分子中含有7个手性碳原子 | |
| D. | 青蒿素在热的酸、碱溶液中均可稳定存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PM2.5是指直径为2.5pm颗粒物 | |
| B. | PM2.5造成的雾霾天气,空气质量很差,对人体健康危害极大 | |
| C. | 空气中的PM2.5,表示每立方米空气中直径小于或等于2.5um的颗粒物的含量,则PM2.5可能导致空气形成气溶胶 | |
| D. | 无风雾霾中的PM2.5的运动应属于布朗运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①② | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
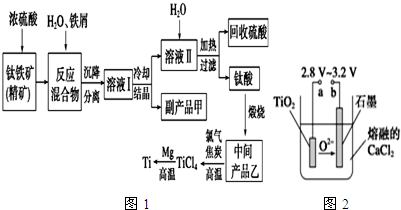
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取用钠、钾、白磷时,没用完的药品要放回原瓶 | |
| B. | 用pH试纸测得氯水的pH为2 | |
| C. | 氯水、硝酸银溶液存放在配有磨口塞的棕色细口瓶中 | |
| D. | 金属钠着火时,用细沙覆盖灭火 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com