Ε‘”ΎΖ¥”ΠAΘ®gΘ©?2BΘ®gΘ©ΓςHΘΨ0Θ§‘ΎΈ¬Ε»ΈΣT
1ΓΔT
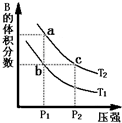
2 ±Θ§ΤΫΚβΧεœΒ÷–BΒΡΧεΜΐΖ÷ ΐΥφ―Ι«Ω±δΜ·ΒΡ«ζœΏ»γΆΦΥυ ΨΘ°ΜΊ¥πœ¬Ν–ΗςΧβΘ°
Θ®1Θ©ΗυΨί«ζœΏΆΦΘ§Ζ÷Έωœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
BC
BC
Θ®ΧνΉ÷ΡΗΘ©Θ°
AΘ°aΓΔcΝΫΒψΒΡΖ¥”ΠΥΌ¬ ΘΚaΘΨc
BΘ°”…Ή¥Χ§bΒΫΉ¥Χ§aΘ§Ω…“‘Ά®ΙΐΦ”»»ΒΡΖΫΖ®
CΘ°bΓΔcΝΫΒψAΤχΧεΒΡΉΣΜ·¬ œύΒ»
Θ®2Θ©…œ ωΖ¥”Π‘ΎΟή±’»ίΤςΘ®Ε®»ίΘ©÷–Ϋχ––Θ§¥οΒΫΤΫΚβΉ¥Χ§ΒΡ±ξ÷Ψ «
BE
BE
Θ®ΧνΉ÷ΡΗΘ©Θ°
AΘ°ΒΞΈΜ ±ΦδΡΎ…ζ≥…n mol AΒΡΆ§ ±Ζ÷Ϋβ2n molB
BΘ°ΝΫ÷÷ΤχΧεΒΡΧεΜΐΖ÷ ΐ≤Μ‘ΌΗΡ±δ
CΘ°v
’ΐΘ®AΘ©=2v
ΡφΘ®BΘ©
DΘ°ΜλΚœΤχΧεΒΡΟήΕ»≤Μ‘ΌΖΔ…ζ±δΜ·
EΘ°ΜλΚœΤχΧεΒΡ―Ι«Ω≤Μ‘ΌΖΔ…ζ±δΜ·
Θ®3Θ©»τ…œ ωΖ¥”Π¥οΤΫΚβ ±Θ§BΤχΧεΒΡΤΫΚβ≈®Ε»ΈΣ0.1mol?L
-1Θ§Ά®ΙΐΦθ–ΓΧεΜΐά¥‘ω¥σΧεœΒΒΡ―Ι«ΩΘ®Έ¬Ε»±Θ≥÷≤Μ±δΘ©Θ§÷Ί–¬¥οΤΫΚβΚσΘ§BΤχΧεΒΡΤΫΚβ≈®Ε»
ΘΨ
ΘΨ
0.1mol?L
-1Θ®ΧνΓΑΘΨΓ±ΓΔΓΑΘΦΓ±ΜρΓΑ=Γ±Θ©Θ°
Θ®4Θ©‘Ύ100Γφ ±Θ§ΫΪ0.40molΒΡBΤχΧε≥δ»κ2L≥ιΩ’ΒΡΟή±’»ίΤς÷–Θ§ΟΩΗτ“ΜΕ® ±ΦδΨΆΕ‘ΗΟ»ίΤςΡΎΒΡΈο÷ Ϋχ––Ζ÷ΈωΘ§ΒΟΒΫ»γœ¬±μΒΡ ΐΨίΘΚ
| ±ΦδΘ®sΘ© |
0 |
20 |
40 |
60 |
80 |
| nΘ®BΘ©/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
| nΘ®AΘ©/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
ΔΌ‘Ύ…œ ωΧθΦΰœ¬Θ§¥”Ζ¥”ΠΩΣ Φ÷Ν40s ±Θ§“‘AΤχΧε±μ ΨΒΡΗΟΖ¥”ΠΒΡΤΫΨυΖ¥”ΠΥΌ¬ ΈΣ
0.000875mol/Θ®L?sΘ©
0.000875mol/Θ®L?sΘ©
ΘΜ
ΔΎ…œ±μ÷–n
3=
=
n
4Θ®ΧνΓΑΘΨΓ±ΓΔΓΑΘΦΓ±ΜρΓΑ=Γ±Θ©Θ§Ζ¥”ΠAΘ®gΘ©?2BΘ®gΘ©‘Ύ100Γφ ±ΒΡΤΫΚβ≥Θ ΐKΒΡ÷ΒΈΣ
0.36
0.36
Θ§…ΐΗΏΈ¬Ε»ΚσΘ§Ζ¥”Π2BΘ®gΘ©?AΘ®gΘ©ΒΡΤΫΚβ≥Θ ΐKΒΡ÷Β
Φθ–Γ
Φθ–Γ
Θ®ΧνΓΑ‘ω¥σΓ±ΓΔΓΑΦθ–ΓΓ±ΜρΓΑ≤Μ±δΓ±Θ©ΘΜ
Δέ»τ‘ΎœύΆ§«ιΩωœ¬Ήν≥θœρΗΟ»ίΤς÷–≥δ»κΒΡ «AΤχΧεΘ§“Σ¥οΒΫ…œ ωΆ§―υΒΡΤΫΚβΉ¥Χ§Θ§AΤχΧεΒΡΤπ Φ≈®Ε»ΈΣ
0.1
0.1
mol?L
-1Θ°


 Ε‘”ΎΖ¥”ΠAΘ®gΘ©?2BΘ®gΘ©ΓςHΘΨ0Θ§‘ΎΈ¬Ε»ΈΣT1ΓΔT2 ±Θ§ΤΫΚβΧεœΒ÷–BΒΡΧεΜΐΖ÷ ΐΥφ―Ι«Ω±δΜ·ΒΡ«ζœΏ»γΆΦΥυ ΨΘ°ΜΊ¥πœ¬Ν–ΗςΧβΘ°
Ε‘”ΎΖ¥”ΠAΘ®gΘ©?2BΘ®gΘ©ΓςHΘΨ0Θ§‘ΎΈ¬Ε»ΈΣT1ΓΔT2 ±Θ§ΤΫΚβΧεœΒ÷–BΒΡΧεΜΐΖ÷ ΐΥφ―Ι«Ω±δΜ·ΒΡ«ζœΏ»γΆΦΥυ ΨΘ°ΜΊ¥πœ¬Ν–ΗςΧβΘ°

