
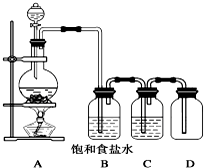
 用下列装置制取并收集纯净的氯气,试回答下列问题:
用下列装置制取并收集纯净的氯气,试回答下列问题:
| ||
| ||


科目:高中化学 来源: 题型:
| A、加入足量纯Cu粉,过滤 |
| B、向溶液中通入足量H2S,过滤 |
| C、向溶液中通入足量C12,再通NH3调节pH值为4左右,过滤 |
| D、向溶液中通入足量C12,再加纯净CuO粉末调节pH值为4左右,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | HA物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgCl2 |
| B、NaOH |
| C、MgSO4 |
| D、NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、糖类物质中只含有C、H、O三种元素 |
| B、蛋白质遇浓硝酸变成紫色 |
| C、油脂在人体中发生水解生成氨基酸 |
| D、糖类、蛋白质都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
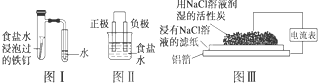
| A、按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管 |
| B、图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁 |
| C、铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-═Cl2↑ |
| D、图Ⅲ装置的总反应为4Al+3O2+6H2O═4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com