
ЁОЬтФПЁПAЁЂBЁЂCЁЂDЁЂE5жжЮЂСЃЃЌЫќУЧПЩФмЪЧдзгЛђРызгЃЌВЂЧвзщГЩЫќУЧЕФдЊЫиЕФдзгађЪ§ЖМаЁгк18ЁЃAЮЂСЃЕФзюЭтВуЕчзгЪ§БШДЮЭтВуЖр5ИіЃЛН№ЪєдзгBЕФдзгКЫФкжЪзгЪ§БШЧАвЛжмЦкЕФЭЌзхдЊЫиЖр8ИіЃЌЦфЕЅжЪВЛФмДгCuSO4ШмвКжажУЛЛГіCuЃЛCдЊЫига3жжЭЌЮЛЫиЃКC1ЁЂC2ЁЂC3ЃЌC1ЕФжЪСПЪ§ЗжБ№ЮЊC2ЁЂC3ЕФ![]() КЭ
КЭ![]() ЃЛDдЊЫиЕФЦјЬЌЧтЛЏЮяШмгкЫЎКѓЯдМюадЃЛEЪЧгЩСНжжВЛЭЌдЊЫизщГЩЕФДјИКЕчКЩЕФЮЂСЃЃЌЫќЙВга2ИідзгКЫ10ИіЕчзгЃЌEМЋвзгыC+НсКЯГЩжаадЮЂСЃЁЃ
ЃЛDдЊЫиЕФЦјЬЌЧтЛЏЮяШмгкЫЎКѓЯдМюадЃЛEЪЧгЩСНжжВЛЭЌдЊЫизщГЩЕФДјИКЕчКЩЕФЮЂСЃЃЌЫќЙВга2ИідзгКЫ10ИіЕчзгЃЌEМЋвзгыC+НсКЯГЩжаадЮЂСЃЁЃ
(1)аДГіЮхжжЮЂСЃЕФБэЪОЗћКХЃКA________ЁЂB________ЁЂC________ЁЂD________ЁЂE________ЁЃ
(2)аДГіCЕФЭЌЮЛЫиУћГЦЃКC1________ЁЂC2________ЁЂC3________ЁЃ
(3)CКЭDаЮГЩЕФ10ИіЕчзгЕФЗжзгЕФЛЏбЇЪНЮЊ________ЁЃ
ЁОД№АИЁП F NaЁЁ HЁЁ NЁЁ OH ы ыЎ ыА NH3
ЁОНтЮіЁПAЮЂСЃЕФзюЭтВуЕчзгЪ§БШДЮЭтВуЖр5ИіЃЌЫЕУїЫќЕФЕчзгВуХХВМЮЊ2ЁЂ7ЃЌЮЊFЃЛН№ЪєдзгBЕФдзгКЫФкжЪзгЪ§БШЧАвЛжмЦкЕФЭЌзхдЊЫиЕФдзгЖр8ИіЃЌЫЕУїЫќЪЧNaЁЂMgЁЂAlжаЕФвЛжжЃЌгжвђВЛФмДгCuSO4ШмвКжажУЛЛГіCuЃЌЫЕУїЦфПЩгыРфЫЎЗДгІЃЌМДBЮЊNaЃЛCдЊЫига3жжЭЌЮЛЫиЃКC1ЁЂC2ЁЂC3ЃЌC1ЕФжЪСПЪ§ЗжБ№ЮЊC2ЁЂC3ЕФ![]() КЭ
КЭ![]() ЃЌЫЕУїЪЧHЕФ3жжЭЌЮЛЫиыЁЂыЎЁЂыАЃЛDдЊЫиЕФЦјЬЌЧтЛЏЮяШмгкЫЎКѓЯдМюадЃЌЫЕУїЪЧАБЦјЃЌDЮЊNЃЛEМЋвзгыC+НсКЯГЩжаадЮЂСЃЃЌC+ЮЊH+ЃЌЫљвдEЮЊOHЁЃ
ЃЌЫЕУїЪЧHЕФ3жжЭЌЮЛЫиыЁЂыЎЁЂыАЃЛDдЊЫиЕФЦјЬЌЧтЛЏЮяШмгкЫЎКѓЯдМюадЃЌЫЕУїЪЧАБЦјЃЌDЮЊNЃЛEМЋвзгыC+НсКЯГЩжаадЮЂСЃЃЌC+ЮЊH+ЃЌЫљвдEЮЊOHЁЃ
(1)аДГіИљОнвдЩЯЗжЮіПЩжЊЮхжжЮЂСЃЕФЗћКХЗжБ№ЪЧFЁЂNaЁЂHЁЂNЁЂOHЁЃ(2)CЕФЭЌЮЛЫиУћГЦЗжБ№ЪЧC1ЪЧыЁЂC2ЪЧыЎЁЂC3ЪЧыАЁЃ(3)CКЭDаЮГЩЕФ10ИіЕчзгЕФЗжзгЕФЛЏбЇЪНЮЊNH3ЁЃ


 ЛЅЖЏгЂгяЯЕСаД№АИ
ЛЅЖЏгЂгяЯЕСаД№АИ УћХЦбЇаЃЗжВужмжмВтЯЕСаД№АИ
УћХЦбЇаЃЗжВужмжмВтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕЊбѕЛЏЮяОпгаВЛЭЌГЬЖШЕФЖОадЃЌЛсЦЦЛЕШЫЬхЕФжаЪрЩёОЃЌГЄЦкЮќШыЛсв§Ц№ФдадТщБдЃЌЪжНХЮЎЫѕЕШЃЌДѓСПЮќШыЪБЛсв§ЗЂжаЪрЩёОТщБдЃЌМЧвфЩЅЪЇЃЌЫФжЋЬБЛОЃЌЩѕжСЫРЭіЕШКѓЙћЁЃЙЙГЩЕчГиЗНЗЈМШФмЪЕЯжгааЇЯћГ§ЕЊбѕЛЏЮяЕФХХЗХЃЌМѕЧсЛЗОГЮлШОЃЌгжФмГфЗжРћгУЛЏбЇФмЃЌЗЂЩњЗДгІ6NO2+8NH3= 7N2+12H2OЃЌзАжУШчЭМЫљЪОЁЃЯТСаЙигкИУЕчГиЕФЫЕЗЈе§ШЗЕФЪЧ ЃЈ ЃЉ
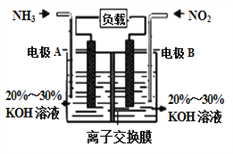
A. ЕчзгДггвВрЕчМЋОЙ§ИКдиКѓСїЯђзѓВрЕчМЋ
B. ЮЊЪЙЕчГиГжајЗХЕчЃЌРызгНЛЛЛФЄашбЁгУвѕРызгНЛЛЛФЄ
C. ЕчМЋAМЋЗДгІЪНЮЊ2NH3-6e-=N2+6H+
D. ЕБга4.48LNO2БЛДІРэЪБЃЌзЊвЦЕчзгЮяжЪЕФСПЮЊ0.8mol
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЃЌНЋЦјЬхXКЭЦјЬхYИї0.16molГфШы10L КуШнУмБеШнЦїжаЃЌЗЂЩњЗДгІЃКXЃЈgЃЉ+YЃЈgЃЉЈT2ZЃЈgЃЉЁїHЃМ0ЃЌвЛЖЮЪБМфКѓДяЕНЦНКтЃЎЗДгІЙ§ГЬжаВтЖЈЕФЪ§ОнШчЯТБэЃКЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
t/min | 2 | 4 | 7 | 9 |
nЃЈYЃЉ/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.ЗДгІЧА2minЕФЦНОљЫйТЪІЭЃЈZЃЉ=2.0ЁС10Љ5 mol/ЃЈLminЃЉ
B.4minЪБЃЌІЭЃЈФцЃЉЃОІЭЃЈе§ЃЉ
C.ИУЮТЖШЯТЃЌДЫЗДгІЕФЦНКтГЃЪ§K=1.44
D.7minЪБЃЌЗДгІЛЙЮДДяЕНЦНКтзДЬЌ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌЯђ20mL 0.2mol/L H2AШмвКжаЕЮМг0.2mol/L NaOHШмвКЃЎгаЙиЮЂСЃЕФЮяжЪЕФСП БфЛЏШчЭМЃЈЦфжаIДњБэH2AЃЌЂђДњБэHAЉ ЃЌ ЂѓДњБэA2ЉЃЉЃЎИљОнЭМЪОХаЖЯЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ 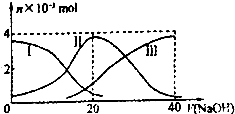
A.ЕБVЃЈNaOHЃЉ=20mLЪБЃЌШмвКжаРызгХЈЖШДѓаЁЙиЯЕ cЃЈNa+ЃЉЃОcЃЈHAЉЃЉЃОcЃЈH+ЃЉЃОcЃЈA2ЉЃЉЃОcЃЈOHЉЃЉ
B.ЕШЬхЛ§ЕШХЈЖШЕФNaOHШмвКгыH2AШмвКЛьКЯКѓЦфШмвКжаЫЎЕФЕчРыГЬЖШБШДПЫЎДѓ
C.гћЪЙNaHAШмвКГЪжаадЃЌПЩвдЯђЦфжаМгШыЫсЛђМю
D.ЯђNaHAШмвКМгШЫЫЎЕФЙ§ГЬжаЃЌpHПЩФмдіДѓвВПЩФмМѕаЁ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвНЩњГЃИјЭбЫЎВЁШЫзЂЩф0.9%ЕФЩњРэбЮЫЎЃЌЖјВЛзЂЩфеєСѓЫЎЛђХЈЖШИќИпЕФХЈбЮЫЎЁЃетЪЧвђЮЊ
A. ЫЎЗжзгШнвзНјГіЯИХм
B. ЮоЛњбЮРызгШнвзНјГіЯИАћ
C. Й§ЖрЛђЙ§ЩйЖМЖдКьЯИАћгаКІ
D. ЮоЛњбЮЖдЮЌГжЯИАћЕФаЮЬЌКЭЩњРэЙІФмгаживЊзїгУ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯЃЌCH3OHвВПЩгЩCOКЭH2КЯГЩЃЎВЮПМКЯГЩЗДгІCOЃЈgЃЉ+2H2ЃЈgЃЉCH3OHЃЈgЃЉЕФЦНКтГЃЪ§ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧ ЃЈЁЁЁЁЃЉ
ЮТЖШ/Ёц | 0 | 100 | 200 | 300 | 400 |
ЦНКтГЃЪ§ | 667 | 13 | 1.9ЁС10Љ2 | 2.4ЁС10Љ4 | 1ЁС10Љ5 |
A.ИУЗДгІе§ЗДгІЪЧЗХШШЗДгІ
B.ИУЗДгІдкЕЭЮТЯТВЛФмздЗЂНјааЃЌИпЮТЯТПЩздЗЂНјааЃЌЫЕУїИУЗДгІЁїSЃМ0
C.дкTЁцЪБЃЌ1LУмБеШнЦїжаЃЌЭЖШы0.1mol COКЭ0.2mol H2 ЃЌ ДяЕНЦНКтЪБЃЌCOзЊЛЏТЪЮЊ50%ЃЌдђДЫЪБЕФЦНКтГЃЪ§ЮЊ100
D.ЙЄвЕЩЯВЩгУЩдИпЕФбЙЧПЃЈ5MPaЃЉКЭ250ЁцЃЌЪЧвђЮЊДЫЬѕМўЯТЃЌдСЯЦјзЊЛЏТЪзюИп
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдзгКЫЭтMЕчзгВуЪєгкзюЭтВуЪБзюЖрШнФЩЕФЕчзгЪ§ЪЧЃЈ ЃЉ
A. 2 B. 8 C. 10 D. 18
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏбЇаЁзщЮЊСЫбаОПЭтНчЬѕМўЖдЛЏбЇЗДгІЫйТЪЕФгАЯьЃЌНјааСЫШчЯТЪЕбщЃК
ЃЈЪЕбщдРэЃЉ2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2Ёќ+8H2O
ЃЈЪЕбщФкШнМАМЧТМЃЉ
ЪЕбщБрКХ | ЪЕбщЮТЖШ | ЪдЙмжаЫљМгЪдМСМАЦфгУСП/mL | ШмвКЭЪжСЮоЩЋЫљашЪБМф/min | |||
0.6mol/L H2C2O4ШмвК | H2O | 3mol/L ЯЁH2SO4ШмвК | 0.05mol/L KMnO4ШмвК | |||
Ђй | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
Ђк | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
Ђл | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
ЃЈ1ЃЉЧыЭъГЩДЫЪЕбщЩшМЦЃЌЦфжаЃКV1=________ЃЌV2=__________ЁЃ
ЃЈ2ЃЉЪЕбщЂйЁЂЂкЬНОПЕФЪЧ_____________ЖдЛЏбЇЗДгІЫйТЪЕФгАЯьЃЌИљОнЩЯБэжаЕФЪЕбщЪ§ОнЃЌПЩвдЕУЕНЕФНсТлЪЧ______________________________________ЁЃ
ЃЈ3ЃЉЬНОПЮТЖШЖдЛЏбЇЗДгІЫйТЪЕФгАЯьЃЌгІбЁдё________________ЃЈЬюЪЕбщБрКХЃЉЁЃ
ЃЈ4ЃЉРћгУЪЕбщ1жаЕФЪ§ОнЃЌМЦЫугУKMnO4БэЪОЕФЛЏбЇЗДгІЫйТЪЮЊ__________ЁЃ
ЃЈ5ЃЉИУаЁзщЭЌбЇИљОнОбщЛцжЦСЫn(Mn2+)ЫцЪБМфБфЛЏЕФЧїЪЦШчЭМ1ЫљЪОЃЌЕЋгаЭЌбЇВщдФвбгаЕФЪЕбщзЪСЯЗЂЯжЃЌИУЪЕбщЙ§ГЬжаn(Mn2+)ЫцЪБМфБфЛЏЕФЪЕМЪЧїЪЦШчЭМ2ЫљЪОЁЃ

ИУаЁзщЭЌбЇИљОнЭМ2ЫљЪОаХЯЂЬсГіСЫаТЕФМйЩшЃЌВЂЩшМЦвдЯТЪЕбщЗНАИМЬајНјааЪЕбщЬНОПЁЃ
ЪЕбщБрКХ | ЪЕбщЮТЖШ/Ёц | ЪдЙмжаЫљМгЪдМСМАЦфгУСП | дйЯђЪдЙмжаМгШыФГжжЙЬЬх | ШмвКЭЪжСЮоЩЋЫљашЪБМф/min | |||
0.6mol/L H2C2O4ШмвК | H2O | 3mol/L ЯЁH2SO4ШмвК | 0.05mol/L KMnO4ШмвК | ||||
Ђм | 25 | 2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t |
ЂйИУаЁзщЭЌбЇЬсГіЕФМйЩшЪЧ__________________________________________ЁЃ
ЂкШєИУаЁзщЭЌбЇЬсГіЕФМйЩшГЩСЂЃЌгІЙлВьЕН_____________________________ЯжЯѓЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзЭщЪЧЬьШЛЦјЕФжївЊГЩЗжЃЌЪЧвЛжжживЊЕФЧхНрФмдДКЭЛЏЙЄдСЯЁЃ
ЃЈ1ЃЉгУУКжЦЬьШЛЦјЪБЛсЗЂЩњЖрИіЗДгІЃЌЭЈЙ§ЖржжЭООЖЩњГЩCH4ЁЃ
вбжЊЃКC(s)+2H2(g)![]() CH4(g) ІЄH=-73kJЁЄmol-1
CH4(g) ІЄH=-73kJЁЄmol-1
2CO(g)![]() C(s)+CO2(g) ІЄH=-171 kJЁЄmol-1
C(s)+CO2(g) ІЄH=-171 kJЁЄmol-1
CO(g)+3H2(g)![]() CH4(g)+H2O (g) ІЄH=-203 kJЁЄmol-1
CH4(g)+H2O (g) ІЄH=-203 kJЁЄmol-1
аДГіCOгыH2O (g)ЗДгІЩњГЩH2КЭCO2ЕФШШЛЏбЇЗНГЬЪН____________________________________ЁЃ
ЃЈ2ЃЉЬьШЛЦјжаКЌгаH2SдгжЪЃЌФГПЦбааЁзщгУАБЫЎЮќЪеЕУЕНNH4HSШмвКЃЌвбжЊTЁцkЃЈNH3H2OЃЉ=1.74ЁС10-5ЃЌk1(H2S)=1.07ЁС10-7ЃЌk2(H2S)=1.74ЁС10-13ЃЌNH4HSШмвКжаЫљКЌСЃзгХЈЖШДѓаЁЙиЯЕе§ШЗЕФЪЧ______________ЁЃ
a.c(NH4+)ЃОc(HS-)ЃОc(OH-)ЃОc(H+) b. c(HS-)ЃОc(NH4+)ЃОc(S2-)ЃОc(H+)
c.c(NH4+)ЃОc(HS-)ЃОc(H2S)ЃОc(H+) d.c(HS-)ЃОc(S2-)ЃОc(H+)ЃОc(OH-)
ЃЈ3ЃЉЙЄвЕЩЯГЃгУCH4гыЫЎеєЦјдквЛЖЈЬѕМўЯТРДжЦШЁH2ЃЌЦфдРэЮЊЃКCH4(g)+H2O(g)![]() CO(g)+3H2(g)ЁЃ
CO(g)+3H2(g)ЁЃ
ЂйвЛЖЈЮТЖШЪБЃЌдквЛИіЬхЛ§ЮЊ2LЕФКуШнУмБеШнЦїжаЃЌМгШы1molCH4КЭ1.4molЫЎеєЦјЗЂЩњЩЯЪіЗДгІЃЌ5minКѓДяЦНКтЃЌЩњГЩ0.2molCOЃЌгУH2БэЪОИУЗДгІЕФЫйТЪЮЊ_______________ЃЌДЫЗДгІЕФЦНКтГЃЪ§ЮЊ__________________(НсЙћБЃСєЕНаЁЪ§ЕуКѓШ§ЮЛ)
ЂкЯТСаЫЕЗЈжаФмЫЕУїДЫЗДгІДяЕНЦНКтзДЬЌЕФЪЧ____________ЁЃ
A.ЬхЯЕЕФбЙЧПВЛдйЗЂЩњБфЛЏ B.ЩњГЩ1mol CH4ЕФЭЌЪБЯћКФ3mol H2
C.ИїзщЗжЕФЮяжЪЕФСПХЈЖШВЛдйИФБф D.ЬхЯЕЕФУмЖШВЛдйЗЂЩњБфЛЏ
E.ЗДгІЫйТЪV(CH4) :V(H2O) :v(CO) :v(H2)= 1:1:1:3
ЃЈ4ЃЉМзДМЫЎеєЦјжиећжЦЧтЗДгІЃКCH3OH(g)+H2O(g)![]() CO2(g) +3H2(g) ІЄH = +49kJЁЄmol-1
CO2(g) +3H2(g) ІЄH = +49kJЁЄmol-1
ЂйЗжЮіЪЪЕБдіДѓЫЎДМБШ[n(H2O) ЁУn (CH3OH)]ЖдМзДМЫЎеєЦјжиећжЦЧтЕФКУДІ____________ЁЃ
ЂкФГЮТЖШЯТЃЌНЋ[n(H2O) ЁУn (CH3OH)]=lЁУ1ЕФдСЯЦјГфШыКуШнУмБеШнЦїжаЃЌГѕЪМбЙЧПЮЊp1ЃЌЗДгІДяЕНЦНКтЪБзмбЙЧПЮЊp2ЃЌдђЦНКтЪБМзДМЕФзЊЛЏТЪЮЊ______________________ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com