
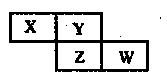
| A.最简单气态氢化物的热稳定性:Y>Z |
| B.最高价氧化物的水化物的酸性:X<W |
| C.X元素的氢化物与其最高价氧化物的水化物能形成离子化合物 |
| D.Y的氢化物沸点远高于Z的氢化物,是因为H-Y键的键能高于H-Z键的键能 |


科目:高中化学 来源:不详 题型:单选题
| A.37Cl与39K具有相同的中子数 |
B.第114号元素的一种核素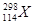 与 与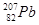 具有相同的最外层电子数 具有相同的最外层电子数 |
| C.H3O+与OH-具有相同的质子数和电子数 |
D.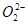 与S2-具有相同的质子数和电子数 与S2-具有相同的质子数和电子数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X>Y>Z | B.Z>Y>X | C.Z>X>Y | D.Y>X>Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:H2Se> H2S> HCl | B.原子半径:Se>P>Si |
| C.酸性:H3PO4>H2SO4>H2SeO4 | D.还原性:Se2->Br->Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期主族元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X能形成化学式为X(OH)3的碱 |
| B.X能与某些金属元素形成化合物 |
| C.X原子的最外层电子数和核电荷数肯定为奇数 |
| D.X可能形成化学式为KXO3的盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com