
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
分析 能与NaHCO3溶液反应生成CO2,说明此分子含有羧基,分子式为C5H8O2说明此分子含有碳碳双键,然后根据官能团的位置异构和碳链异构确定,以此解答该题.
解答 解:由该有机物的化学性质和组成判断其含有碳碳双键和羧基,
当没有支链时,其碳骨架有3种:CH2=CH2CH2CH2COOH,CH3CH=CHCH2-COOH,CH3CH2CH=CHCOOH,
有一个甲基做支链的结构有4种:CH2=CH(CH3)CH2COOH,CH2=CHCH(CH3)COOH,(CH3)2CH=CHCOOH,CH3CH=CH(CH3)COOH,
有一个乙基做支链的结构有1种:CH2=C(CH2CH3)COOH,
总共8种.
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与推断能力的考查,注意羧酸、烯烃的性质,题目难度不大.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是以烃A为原料经过一系列反应合成的:
)是以烃A为原料经过一系列反应合成的:

 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaCl+2H2O.
+2NaCl+2H2O. +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
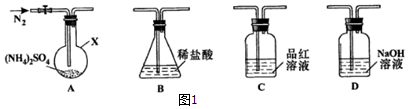
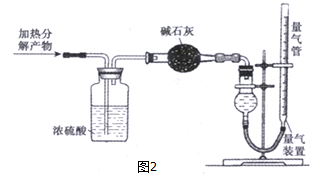
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第三次月考化学试卷(解析版) 题型:选择题
在含c(NH4Cl)=3c(AlCl3)的溶液中滴加稀NaOH溶液。下列离子方程式不符合实际情况的是( )
A.Al3++3NH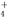 +6OH-===Al(OH)3↓+3NH3·H2O
+6OH-===Al(OH)3↓+3NH3·H2O
B.2Al3++NH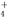 +7OH-===2Al(OH)3↓+NH3·H2O
+7OH-===2Al(OH)3↓+NH3·H2O
C.Al3++3NH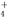 +7OH-===AlO
+7OH-===AlO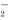 +3NH3·H2O+2H2O
+3NH3·H2O+2H2O
D.Al3++5NH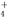 +9OH-===5NH3·H2O+AlO
+9OH-===5NH3·H2O+AlO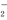 +7H2O
+7H2O
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上学期第二次月考化学试卷(解析版) 题型:实验题
(NH4)2Fe( SO4)2·6H2O(硫酸亚铁铵的结晶水合物)是重要的化工原料和化学试剂,在空气中长期放置会被氧化而变质。某课题小组为了探究莫尔盐的分解产物,开展了如下实验:
SO4)2·6H2O(硫酸亚铁铵的结晶水合物)是重要的化工原料和化学试剂,在空气中长期放置会被氧化而变质。某课题小组为了探究莫尔盐的分解产物,开展了如下实验:
已知:五氧化二磷是酸性干燥剂,假设干燥管中试剂均足量。
(1)甲同学设计如下实验检验(NH4)2Fe(SO4)2·6H2O分解的部分产物。装置A的气密性的检查方法是 。
①B装置的作用是 。
②M干燥管中所放的药品是 。
(2)检验(NH4)2Fe(SO4)2·6H2O是否变质的试剂是 (填化学式);检验是否完全变质的实验方法是 。
(3)实验室常用(NH4)2Fe(SO4)2·6H2O标准溶液测定过二硫酸铵[(NH4)2S2O8]的纯度(过二硫酸铵的相对分子量为238,滴定反应的离子方程式为:S2O82-+2Fe2+  2Fe3++2SO42-)。取w g过二硫酸铵样品溶于蒸馏水配制成250 mL 溶液。准确量取20.00 mL配制的溶液于锥形瓶中,用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,重复进行三次平行实验,测得有关数据如表所示:
2Fe3++2SO42-)。取w g过二硫酸铵样品溶于蒸馏水配制成250 mL 溶液。准确量取20.00 mL配制的溶液于锥形瓶中,用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,重复进行三次平行实验,测得有关数据如表所示:
实验序号 | 起始读数/mL | 终点读数/mL |
Ⅰ | 2.50 | 22.58 |
Ⅱ | 1.00 | 23.12 |
Ⅲ | 0.00 | 19.92 |
①完成上述实验需要准确量取20.00 mL过二硫酸铵溶液,所用仪器的名称是 。
②根据上述数据计算,样品的纯度为  (用含w、c的代数式表示)。
(用含w、c的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com