
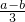
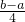
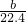 mol��L-1��
mol��L-1�� ���������Ũ�ȣ�
���������Ũ�ȣ�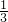 ��a-4b��mol=
��a-4b��mol=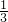 ��a-b��mol��
��a-b��mol��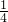 amol����NO��Ӧ������Ϊbmol-
amol����NO��Ӧ������Ϊbmol-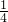 amol��NO��ȫ��Ӧ��Ҫ����Ϊ
amol��NO��ȫ��Ӧ��Ҫ����Ϊ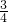 bmol������NOʣ�࣬��
bmol������NOʣ�࣬��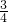 bmol��bmol-
bmol��bmol-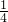 amol������a��b��
amol������a��b��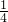 a��mol������Ӧ��NOΪ
a��mol������Ӧ��NOΪ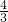 ��b-
��b-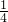 a��mol����ʣ��NOΪbmol-
a��mol����ʣ��NOΪbmol-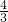 ��b-
��b-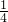 a��mol=
a��mol=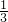 ��a-b��mol��
��a-b��mol��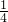 amol��NO��Ҫ����Ϊ
amol��NO��Ҫ����Ϊ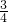 bmol����Ϊ
bmol����Ϊ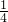 amol+
amol+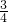 bmol��bmol��������a��b��ʣ������Ϊbmol-��
bmol��bmol��������a��b��ʣ������Ϊbmol-��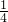 amol+
amol+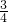 bmol��=
bmol��=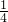 ��b-a��mol���ʢ���ȷ
��b-a��mol���ʢ���ȷ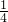 amol��NO��Ҫ����Ϊ
amol��NO��Ҫ����Ϊ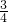 bmol
bmol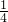 amol+
amol+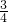 bmol=bmol��������a=b������NԪ���غ�n��HNO3��=n��NO��+n��NO2��=��a+b��mol����Һ�������NO��NO2�����֮��Ϊ��a+b��mol��22.4L/mol=22.4��a+b���������Ũ��Ϊ
bmol=bmol��������a=b������NԪ���غ�n��HNO3��=n��NO��+n��NO2��=��a+b��mol����Һ�������NO��NO2�����֮��Ϊ��a+b��mol��22.4L/mol=22.4��a+b���������Ũ��Ϊ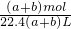 =
=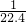 mol/L���ʢ۴���
mol/L���ʢ۴���

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| a-b |
| 3 |
| b-a |
| 4 |
| b |
| 22.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��ȫ��������У�߿���ѧʾ���Ծ��������棩 ���ͣ�ѡ����
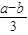
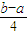
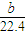 mol��L-1��
mol��L-1���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com