
Į×¼°Ęä»ÆŗĻĪļŌŚæĘŃŠ¼°Éś²śÖŠ¾łÓŠ×ÅÖŲŅŖµÄÓ¦ÓĆ”£
£Ø1£©ŗģĮ×P(s)ŗĶCl2 (g)·¢Éś·“Ӧɜ³ÉPCl3(g)ŗĶ PCl5(g)£¬·“Ó¦¹ż³ĢČēĻĀ”£
2P(s) + 3Cl2(g) = 2PCl3(g) ”÷H=£612kJ/mol
2P(s) + 5Cl2(g) = 2PCl5(g) ”÷H=£798kJ/mol
ĘųĢ¬PCl5Éś³ÉĘųĢ¬PCl3ŗĶCl2µÄČČ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©æÉÄę·“Ó¦PCl3(g)+Cl2(g) PCl5(g) 2E(g)
PCl5(g) 2E(g) F(g)+G(g)·Ö±šŌŚĆܱÕČŻĘ÷µÄĮ½øö·“Ó¦ŹŅÖŠ½ųŠŠ£¬·“Ó¦ŹŅÖ®¼äÓŠæÉ»¬¶Æ”¢ĪŽÄ¦²ĮµÄĆÜ·āøō°å”£·“Ó¦æŖŹ¼ŗĶ“ļµ½Ę½ŗāŹ±ÓŠ¹ŲĪļĄķĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ
F(g)+G(g)·Ö±šŌŚĆܱÕČŻĘ÷µÄĮ½øö·“Ó¦ŹŅÖŠ½ųŠŠ£¬·“Ó¦ŹŅÖ®¼äÓŠæÉ»¬¶Æ”¢ĪŽÄ¦²ĮµÄĆÜ·āøō°å”£·“Ó¦æŖŹ¼ŗĶ“ļµ½Ę½ŗāŹ±ÓŠ¹ŲĪļĄķĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ

¢Ł“ļµ½Ę½ŗāIŹ±£¬ĢåĻµŃ¹ĒæÓė·“Ó¦æŖŹ¼Ź±ĢåĻµŃ¹ĒæÖ®±ČĪŖ ”£
¢ŚĘ½ŗāIµ½Ę½ŗāIIµÄĢõ¼ž¢ŁŹĒ £ØĢī”°ÉżĪĀ”±»ņ”°½µĪĀ”±£©”£
£Ø3£©ŃĒĮ×Ėį£ØH3PO3£©Óė×ćĮæµÄNaOHČÜŅŗ·“Ӧɜ³ÉNa2HPO3”£µē½āNa2HPO3ČÜŅŗŅ²æɵƵ½ŃĒĮ×Ėį£¬×°ÖĆČēĶ¼ĖłŹ¾£ŗ
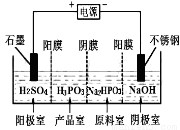
Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ________________£»²śĘ·ŹŅÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø4£©Ņ»¶ØĪĀ¶ČĻĀ£¬Ksp [Mg3(PO4)2] =6.0”Į10-29£¬Ksp [Ca3(PO4)2] =6.0”Į10-26”£ĻņÅØ¶Č¾łĪŖ0.20 mol”¤L£1µÄMgCl2ŗĶCaCl2»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČėNa3PO4£¬ĻČÉś³É ³Įµķ£ØĢī»ÆѧŹ½£©£»µ±²āµĆČÜŅŗĘäÖŠŅ»ÖÖ½šŹōŃōĄė×Ó³ĮµķĶźČ«£ØÅØ¶ČŠ”ÓŚ10-5mol/L£©Ź±£¬ČÜŅŗÖŠµÄĮķŅ»ÖÖ½šŹōŃōĄė×ÓµÄĪļÖŹµÄĮæÅضČc= mol/L”£

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģĢģ½ņŅ»ÖŠøßČżÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®ÅØĻõĖįÓė×ćĮæĶʬ·“Ó¦Ź±£¬ĻČÉś³Éŗģ×ŲÉ«ĘųĢ壬ŗóÉś³ÉĪŽÉ«ĘųĢå
B£®Ńõ»ÆĀĮµÄČŪµćŗÜøߣ¬æÉÓĆÓŚÖĘŌģČŪČŚÉÕ¼īµÄŪįŪö
C£®ŌŚŗ¬FeCl2ŌÓÖŹµÄFeCl3ČÜŅŗÖŠĶØČė×ćĮæCl2ŗ󣬳ä·Ö¼ÓČČ³żČ„¹żĮæµÄCl2£¬²»ÄܵƵ½“æ¾»µÄFeC13ČÜŅŗ
D£®±„ŗĶĀČĖ®¼ČÓŠĖįŠŌÓÖÓŠĘư׊Ō£¬¼ÓČėŹŹĮæNaHCO3¹ĢĢ壬ĘäĘư׊ŌŌöĒæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”øßČżŠ”¶žµ÷æ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Al”¢Fe”¢Cu¶¼ŹĒÖŲŅŖµÄ½šŹōŌŖĖŲ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ČżÕ߶ŌÓ¦µÄŃõ»ÆĪļ¾łĪŖ¼īŠŌŃõ»ÆĪļ
B£®ČżÕߵĵ„ÖŹ·ÅÖĆŌŚæÕĘųÖŠ¾łÖ»Éś³ÉŃõ»ÆĪļ
C£®Fe2O3 ÓėFe3O4»„ĪŖĶ¬ĖŲŅģŠĪĢå
D£®³£ĪĀĻĀČżÕß¼ÓČėÅØĮņĖįÖŠ¾łĪŽĆ÷ĻŌĻÖĻó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”øßČżŠ”¶žµ÷æ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÄÜÕżČ·±ķŹ¾ĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½µÄŹĒ£Ø £©
A£®Ļņ ČÜŅŗÖŠ¼ÓČėÉŁĮæĀČĖ®
ČÜŅŗÖŠ¼ÓČėÉŁĮæĀČĖ®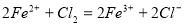
B£®NaClO (aq) ÖŠĶØČė¹żĮæ SO2: C1O- + SO2 + H2O = HClO +HSO3-
C£®ĀČĘųĶØČėĖ®ÖŠ£ŗCl2+H2O=2H++Cl-+ ClO-
D£®“ĪĀČĖįøĘČÜŅŗÖŠĶØČėÉŁĮæCO2£ŗCa2++2ClO-+H2O+CO2=CaCO3”ż+2 HClO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”øßČżŠ”¶žµ÷æ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®øł¾Ż·“Ó¦5Fe2++MnO4”„+8H+=5Fe3++Mn2++4H2OæÉÖŖ£ŗÓĆĖįŠŌKMnO4ČÜŅŗæɼģŃéĀĢ·Æ£ØFeSO4”¤7H2O£©ŹĒ·ń±äÖŹ
B£®øł¾Ż·“Ó¦Fe+4HNO3=Fe(NO3)2+2NO”ü+2H2OæÉÖŖ£ŗ·“Ó¦ÖŠHNO3±ķĻÖĖįŠŌŗĶŃõ»ÆŠŌ
C£®øł¾Ż·“Ó¦CuSO4+H2S=CuS”ż+H2SO4æÉÖŖ£ŗH2SµÄĖįŠŌ±ČH2SO4Ēæ
D£®øł¾Ż·“Ó¦H3PO3+2NaOH(×ćĮæ)=Na2HPO3+2H2OæÉÖŖ£ŗH3PO3ŹōÓŚČżŌŖĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”µČĪ劣øßČżÉĻѧʌµŚŅ»“ĪÄ£Äā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¼×”¢ŅŅ”¢±ū”¢¶”¾łĪŖ֊ѧ»Æѧ֊³£¼ūµÄµ„ÖŹ»ņ»ÆŗĻĪļ£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£Ø²æ·Ö²śĪļŅŃĀŌČ„£©£¬ĻĀĮŠø÷×éĪļÖŹÖŠ²»ÄÜ°“Ķ¼Ź¾¹ŲĻµ×Ŗ»ÆµÄŹĒ
Ń”Ļī | ĪļÖŹ×Ŗ»Æ¹ŲĻµ | ¼× | ŅŅ | ±ū | ¶” |
A |
| NaOH | NaHCO3 | Na2CO3 | CO2 |
B | AlCl3 | NaAlO2 | Al(OH)3 | NaOH | |
C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 | |
D | C | CO | CO2 | O2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”µČĪ劣øßČżÉĻѧʌµŚŅ»“ĪÄ£Äā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
20”ꏱ£¬PbCl2(s)ŌŚ²»Ķ¬ÅضČŃĪĖįÖŠµÄ×ī“óČܽāĮæ(µ„Ī»£ŗg”¤L£1)ČēÓŅĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
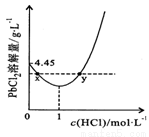
A£®ŃĪĖįÅضČŌ½“ó£¬Ksp(PbCl2)Ō½“ó
B£®PbCl2ÄÜÓėŅ»¶ØÅØ¶ČµÄŃĪĖį·“Ó¦
C£®x”¢yĮ½µć¶ŌÓ¦µÄČÜŅŗÖŠc(Pb2+)ĻąµČ
D£®Ķłŗ¬Pb2+µÄČÜŅŗÖŠ¼ÓČė¹żĮæÅØŃĪĖį£¬æɽ«Pb2+ĶźČ«×Ŗ»ÆĪŖPbCl2(s)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ¹ć¶«Ź”øßČżÉĻѧʌæŖŃ§æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ļņŗ¬ÓŠMgCO3¹ĢĢåµÄČÜŅŗÖŠµĪ¼ÓÉŁŠķÅØŃĪĖį£ØŗöĀŌĢå»ż±ä»Æ£©£¬ĻĀĮŠŹżÖµ±äŠ”µÄŹĒ
A£®c(CO32?) B£®c(Mg2+) C£®c(H+) D£®Ksp(MgCO3)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ¹ć¶«Ź”øßŅ»ÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓūŹ¹1L 0.5mol/LµÄNaOHČÜŅŗµÄÅضČŌö“óŅ»±¶£¬æɲÉČ”µÄŗĻĄķ“ėŹ©ŹĒ( )
A£®¼ÓČė20g ¹ĢĢåNaOH£¬½Į°č”¢Čܽā
B£®½«ČÜŅŗ¼ÓČČÅØĖõÖĮ0.2L
C£®¼ÓČė10mol/LµÄNaOHČÜŅŗ0.1 L£¬ŌŁĻ”ŹĶÖĮ1.5 L
D£®¼ÓČė1 L 1.5 mol/LµÄNaOHČÜŅŗ»ģŗĻ¾łŌČ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com