
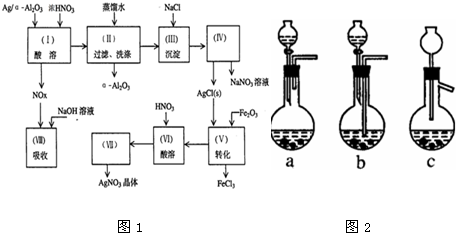
分析 由于α-Al2O3不溶于稀硝酸,Ag/a-Al2O3中加入稀硝酸后银溶解生成硝酸银,过滤后,滤液中含有AgNO3,滤渣为α-Al2O3,滤液中加入NaCl得到沉淀为AgCl,再过滤分离得到AgNO3与NaNO3溶液,AgCl转化为Ag2O,溶解过滤分离,再用硝酸溶解Ag2O得到AgNO3,蒸发浓缩、冷却结晶、过滤等得到AgNO3晶体.
(1)反应生成氮的氧化物气体,需要导出用氢氧化钠溶液吸收,装置应密闭,出气管不能在液面以下;
Ag与浓硝酸反应生成硝酸银、二氧化氮与水,随反应计算,浓硝酸变稀,Ag与稀硝酸反应生成硝酸银、NO与水;
(2)自来水中含有氯气,氯气与水反应生成HCl与HClO,HCl与AgNO3反应生成AgCl与HNO3;
(3)第(Ⅵ)步是Ag2O与HNO3反应生成AgNO3与水;
(4)从溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤等操作.
解答 解:由于α-Al2O3不溶于稀硝酸,Ag/a-Al2O3中加入稀硝酸后银溶解生成硝酸银,过滤后,滤液中含有AgNO3,滤渣为α-Al2O3,滤液中加入NaCl得到沉淀为AgCl,再过滤分离得到AgNO3与NaNO3溶液,AgCl转化为Ag2O,溶解过滤分离,再用硝酸溶解Ag2O得到AgNO3,蒸发浓缩、冷却结晶、过滤等得到AgNO3晶体.
(1)反应生成氮的氧化物气体,需要导出用氢氧化钠溶液吸收,装置b中产生的气体不能导出,会导致装置内压强增强,发生炸裂的危险,c装置不密闭,故选a;
Ag与浓硝酸反应生成硝酸银、二氧化氮与水,随反应计算,浓硝酸变稀,Ag与稀硝酸反应生成硝酸银、NO与水,反应方程式为:Ag+2HNO3(浓)=AgNO3+NO2↑+H2O、3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O,
故答案为:a;Ag+2HNO3(浓)=AgNO3+NO2↑+H2O、3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O;
(2)自来水中含有氯气,氯气与水反应生成HCl与HClO,HCl与AgNO3反应生成AgCl与HNO3,反应离子方程式为:Ag++Cl-=AgCl↓,
故答案为:Ag++Cl-=AgCl↓;
(3)第(Ⅵ)步是Ag2O与HNO3反应生成AgNO3与水,反应方程式为:Ag2O+2HNO3=2AgNO3+H2O,
故答案为:Ag2O+2HNO3=2AgNO3+H2O;
(4)从AgNO3溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤等操作,顺序为BED,
故答案为:B、E、D.
点评 本题考查制备方案工艺流程、物质的分离提纯、对原理的分析理解等,关键是明确工艺流程中每一步中的试剂、操作与原理,是对学生综合能力的考查,难度中等.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 18gD2O中含的质子数为9 NA | |
| B. | 1.00molNaCl中,所有Na+的最外层电子总数为10×6.02×1023 | |
| C. | 46gNO2和N2O4混合气体中含有原子总数为3 NA | |
| D. | 1molNa 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
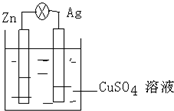 (1)在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是氧化反应(“氧化”或“还原”).电极反应式为Zn-2e-═Zn2+.
(1)在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是氧化反应(“氧化”或“还原”).电极反应式为Zn-2e-═Zn2+.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
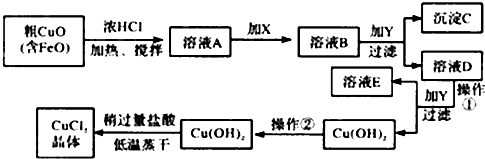
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅单质广泛用于制作光导纤维 | |
| B. | SO2使氯水褪色,说明SO2具有漂白性 | |
| C. | 氯气泄漏后应顺风向低处跑 | |
| D. | 酸雨的pH值小于5.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对分子质量相同而结构不同的化合物互称为同分异构体 | |
| B. | 分子式相同而结构不同的化合物互称为同分异构体 | |
| C. | 同分异构体之间由于分子组成相同,所以它们的性质相同 | |
| D. | 只有少数的有机物之间存在同分异构现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com