
| 原子 | 核电荷数 | 质量数 | 质子数 | 中子数 | 电子数 | 核外电子数 |
| A | 4 | 8 | ||||
| B | 6 | 8 | ||||
| C | 12 | 2、8、1 | ||||
| D | 16 | 16 | ||||
| E | 16 | 8 | ||||
| F | 27 | 2、8、3 |

 .
. 分析 原子中,中子数+质子数=质量数,质子数=核外电子数,以此解答该题.
解答 解:原子中,中子数+质子数=质量数,质子数=核外电子数,如表填满,应为:
| 原子 | 核电荷数 | 质量数 | 质子数 | 中子数 | 电子数 | 核外电子数 |
| A | 4 | 8 | 4 | 4 | 4 | 2、2 |
| B | 6 | 14 | 6 | 8 | 6 | 2、4 |
| C | 11 | 23 | 11 | 12 | 11 | 2、8、1 |
| D | 16 | 32 | 16 | 16 | 16 | 2、8、6 |
| E | 8 | 16 | 8 | 8 | 8 | 2、6 |
| F | 13 | 27 | 13 | 14 | 13 | 2、8、3 |
 ,故答案为:
,故答案为: ;
; ,故答案为:
,故答案为: .
.点评 本题考查原子结构与性质,为高频考点,侧重于学生的分析能力的考查,注意把握原子结构特点,把握质子数、质量数与核外电子数的关系,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 苯酚能跟 NaOH 溶液反应,乙醇不能与 NaOH 溶液反应 | |
| B. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| D. | 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液水解的离子方程式:CO32-+2H2O=H2CO3+2OH- | |
| B. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| C. | 氢氧化钡在水溶液中的电离方程式:Ba(OH)2=Ba2++2OH- | |
| D. | 向含Al(OH)3白色沉淀的溶液中不断通CO2沉淀逐渐溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 随着电解的进行,溶液的pH减小 | |
| B. | OH-向阳极移动,阳极附近溶液呈碱性 | |
| C. | 阴极上H+得电子被还原成H2 | |
| D. | NO3-向阳极移动,K+向阴极移动,分别在对应的电极上析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 质量相等时,三种气体所含原子数相等 | |
| B. | 质量相等时,三种气体所含氮原子数相等 | |
| C. | 所含氮原子数相等时,三种气体的质量相等 | |
| D. | 质量相等时,二氧化氮所含氧原子数比一氧化氮所含氧原子数多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液(KSCN) | B. | KOH(盐酸) | ||
| C. | Na2SO3溶液(BaCl2) | D. | HCHO溶液(石蕊试液) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
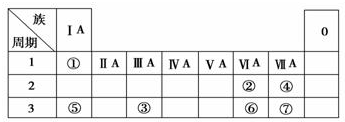
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
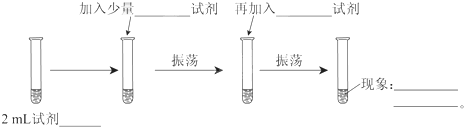
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com