
| 实验次数 | 镁带质量(g) | 测得气体的体积(L) |
| 1 | 18.000 | 16.90 |
| 2 | 18.000 | 17.00 |
| 16.90L+17.00L |
| 2 |
| m(镁) |
| m(总质量) |
| 18.000g |
| 24g/mol |
| 16.90L+17.00L |
| 2 |
|
| 0.73×24 |
| 18.000 |


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
| A、反应达到平衡时,降低温度,平衡逆向移动 |
| B、使用催化剂,正反应速率增大,逆反应速率减小 |
| C、若反应体系温度不再变化,说明反应达到平衡状态 |
| D、减小SO2的浓度,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
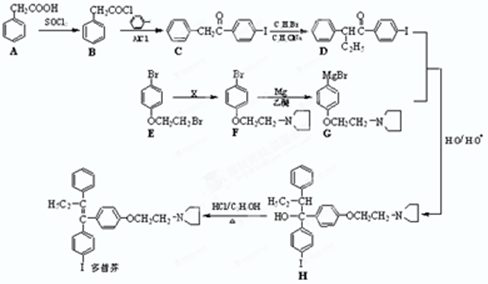
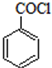 )是合成药品的重要中间体.请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
)是合成药品的重要中间体.请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 氯气 |
| ① |
| 一定条件 |
| ② |
| 高温、高压、催化剂 |
| ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 纯碱中常含有少量氯化钠,请设计实验测定纯碱中Na2CO3的质量分数.根据你所设计的方案中的有关的数据,写出纯碱中Na2CO3的质量分数的表达式.
纯碱中常含有少量氯化钠,请设计实验测定纯碱中Na2CO3的质量分数.根据你所设计的方案中的有关的数据,写出纯碱中Na2CO3的质量分数的表达式.查看答案和解析>>
科目:高中化学 来源: 题型:
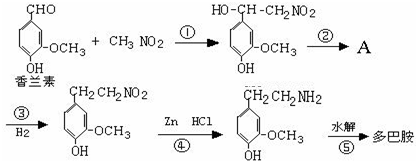
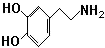 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
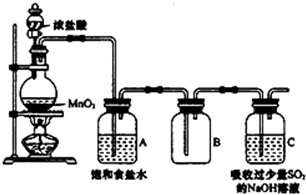 某科研小组用MnO2的浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对尾气进行吸收处理,如图所示:
某科研小组用MnO2的浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对尾气进行吸收处理,如图所示:| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol/L H2SO4溶液至溶液呈酸性,然后将所得溶液分别置于A、B试管中 | / |
| 步骤2: | Ⅰ: Ⅱ: |
| 步骤3: | Ⅰ: Ⅱ: |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、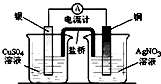 装置可将化学能转化为电能 |
B、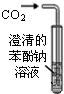 装置可用于比较碳酸、苯酚酸性的强弱 |
C、 装置可用来进行浓硫酸的稀释 |
D、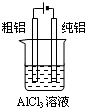 装置可用于电解精炼铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com