
全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。下图是钒电池基本工作原理示意图:
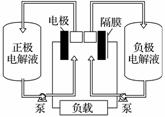
请回答下列问题:
(1)硫酸在电池技术和实验室中具有广泛的应用,在传统的铜锌原电池中,硫酸是____________,实验室中配制硫酸亚铁时需要加入少量硫酸,硫酸的作用是____。
(2)钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、VO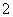 )为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O
)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O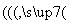 V2++VO
V2++VO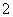 +2H+。放电时的正极___________________________________________________________________,
+2H+。放电时的正极___________________________________________________________________,
充电时的阴极反应式为___________________________________________________________。放电过程中,电解液的pH________(填“升高”、“降低”或“不变”)。
(3)钒电池基本工作原理示意图中“正极电解液”可能是________(填字母)。
a.VO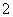 、VO2+混合液 b.V3+、V2+混合液
、VO2+混合液 b.V3+、V2+混合液
c.VO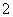 溶液 d.VO2+溶液
溶液 d.VO2+溶液
e.V3+溶液 f.V2+溶液
(4)能够通过钒电池基本工作原理示意图中“隔膜”的离子是________________________________________________________________________。
答案 (1)电解质溶液 抑制硫酸亚铁的水解
(2)VO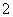 +2H++e-===VO2++H2O V3++e-===V2+ 升高 (3)acd (4)H+
+2H++e-===VO2++H2O V3++e-===V2+ 升高 (3)acd (4)H+
解析 (1)传统的铜锌原电池中,锌与酸反应生成氢气,故硫酸为电解质溶液;硫酸亚铁容易水解,且水解显酸性,加入少量硫酸,可以抑制其水解变质。
(2)正极反应是还原反应,由电池总反应可知放电时的正极反应为VO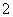 +2H++e-===VO2++H2O;充电时,阴极反应为还原反应,故为V3+得电子生成V2+的反应。
+2H++e-===VO2++H2O;充电时,阴极反应为还原反应,故为V3+得电子生成V2+的反应。
(3)充电时阳极反应式为VO2++H2O-e-===VO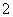 +2H+,故充电完毕的正极电解液为VO
+2H+,故充电完毕的正极电解液为VO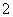 溶液,而放电完毕的正极电解液为VO2+溶液,故正极电解液可能是选项a、c、d。
溶液,而放电完毕的正极电解液为VO2+溶液,故正极电解液可能是选项a、c、d。
(4)充电和放电过程中,正极电解液与负极电解液不能混合,起平衡电荷作用的是加入的酸,故H+可以通过隔膜。


科目:高中化学 来源: 题型:
在水中加入等物质的量的Ag+、Pb2+、Na+、SO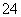 、NO
、NO 、Cl-,该溶液放在用惰性电极材料作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
、Cl-,该溶液放在用惰性电极材料作电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为( )
A.35.5∶108 B.16∶207
C.8∶1 D.108∶35.5
查看答案和解析>>
科目:高中化学 来源: 题型:
能量之间可相互转化:电解食盐水制备Cl2是将电能转化为化学能,而原电池可将化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。

①完成原电池甲的装置示意图(见上图),并作相应标注,要求:在同一烧杯中,电极与溶液含相同的金属元素。
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极__________。
③甲乙两种原电池可更有效地将化学能转化为电能的是________,其原因是_____________。
④根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在上述的材料中应选__________作阳极。
(2)[2013·北京理综,26(4)]通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
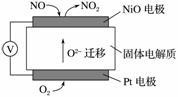
①Pt电极上发生的是________反应(填“氧化”或“还原”)
②写出NiO电极的电极反应式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是( )
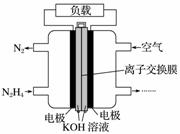
A.电流从右侧电极经过负载后流向左侧电极
B.负极发生的电极反应式为N2H4+4OH--4e-===N2+4H2O
C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D.该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
KHSO4、BaCl2、Na2CO3、FeSO4和氯水五种溶液,如图所示的相互反应,图中每条连线两端的物质可以发生化学反应。下列说法不合理的是( )
A.X一定为KHSO4
B.Y一定为Na2CO3
C.Z可能是氯水
D.M、N必定各为BaCl2、FeSO4中的一种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方程式①AgCl(s)Ag+(aq)+Cl-(aq)、
②AgCl===Ag++Cl-、 ③CH3COOHCH3COO-+H+各表示什么意义?
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知:pM=-lg c(M),p(CO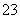 )=-lg c(CO
)=-lg c(CO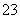 )。下列说法正确的是( )
)。下列说法正确的是( )
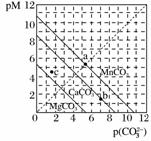
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO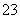 )
)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO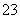 )
)
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO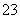 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
N2在诸多领域用途广泛。某化学兴趣小组为探究在实验室制备较为纯净N2的方法,进行了认真的准备。请你参与交流与讨论。
[查阅资料]N2的制法有下列三种方案:
方案1:加热NaNO2和NH4Cl的浓溶液制得N2。
方案2:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉。
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2。
[实验准备]以实验室常见仪器(药品)等设计的部分装置如下图(部分夹持和加热仪器未画出)。
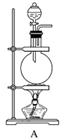
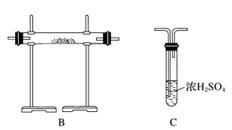

[分析交流]
(1)若以方案1制得N2,应选择的发生装置是___________________________。
(2)若按方案2制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的连接顺序是______________(填字母)。获得N2的反应原理是________________________________________________________________________(写反应方程式)。
(3)若以排水法收集N2,其中会混入水蒸气。但也不宜用排空气法,其原因是________________________________________________________________________。
你提出的收集方法是______________________________________。
(4)上述三个方案中,制得的N2纯度最差的是________。在N2纯度要求不甚严格的情况下,有人建议将方案2和方案3结合使用,你认为其优点是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com