
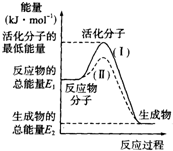
 £Ø1£©ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó±»³ĘĪŖ»ī»Æ·Ö×Ó£®Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčŅŖĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJ•mol-1±ķŹ¾£®ĒėČĻÕę¹Ū²ģĻĀĶ¼£¬Č»ŗó»Ų“šĪŹĢā£®
£Ø1£©ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó±»³ĘĪŖ»ī»Æ·Ö×Ó£®Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčŅŖĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJ•mol-1±ķŹ¾£®ĒėČĻÕę¹Ū²ģĻĀĶ¼£¬Č»ŗó»Ų“šĪŹĢā£®·ÖĪö £Ø1£©ŅĄ¾ŻĶ¼Ļó·ÖĪö·“Ó¦ĪļµÄÄÜĮæ“óÓŚÉś³ÉĪļµÄÄÜĮ棬·“Ó¦·ÅČČ£»ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅÄÜ·¢Éś»Æѧ·“Ó¦£¬ĖłŅŌŠčŅŖÄÜĮ棻·“Ó¦µÄģŹ±ä=Éś³ÉĪļµÄÄÜĮæ-·“Ó¦ĪļµÄÄÜĮ棻
£Ø2£©ÖŠŗĶČȵÄøÅÄī£ŗĻ”µÄĒæĖįŗĶĒæ¼ī·“Ӧɜ³É1molĖ®Ėł·Å³öµÄČČĮæĒó³öÖŠŗĶČČ£¬ŅŌ“ĖŹéŠ“ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½
£Ø3£©øł¾ŻČČ»Æѧ·½³ĢŹ½µÄŹéŠ“·½·ØæÉÖŖ£¬»Æѧ¼ĘĮæŹżÓė·“Ó¦ČČ³ÉÕż±Č£¬²¢×¢Ņā±źĆ÷ĪļÖŹµÄ¾Ū¼ÆדĢ¬£»
£Ø4£©øł¾ŻøĒĖ¹¶ØĀÉ·ÖĪö½ā“š£®
½ā“š ½ā£ŗ£Ø1£©ŅĄ¾ŻĶ¼Ļó·ÖĪö·“Ó¦ĪļµÄÄÜĮæ“óÓŚÉś³ÉĪļµÄÄÜĮ棬·“Ó¦·ÅČČ£»ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅÄÜ·¢Éś»Æѧ·“Ó¦£¬ĘäĖūŠčŅŖÄÜĮ棻·“Ó¦µÄģŹ±ä=Éś³ÉĪļµÄÄÜĮæ-·“Ó¦ĪļµÄÄÜĮæØTE2-E1£»
¹Ź“š°øĪŖ£ŗ·ÅČČ£¬ŠčŅŖ£¬E2-E1 £»
£Ø2£©1.00L 1.00mol/L H2SO4ČÜŅŗÓė2.00L 1.00mol/L NaOHČÜŅŗĶźČ«·“Ó¦£¬·Å³ö114.6kJµÄČČĮ棬¼“Éś³É2molĖ®·Å³ö114.6kJµÄČČĮ棬·“Ó¦µÄ·“Ó¦ČČĪŖ-11.46kJ/mol£¬ÖŠŗĶČČĪŖ-57.3kJ/mol£¬ŌņÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½£ŗNaOH£Øaq£©+$\frac{1}{2}$H2SO4£Øaq£©=$\frac{1}{2}$Na2SO4£Øaq£©+H2O£Øl£©”÷H=-57.3kJ/mol£¬
¹Ź“š°øĪŖ£ŗNaOH£Øaq£©+$\frac{1}{2}$H2SO4£Øaq£©=$\frac{1}{2}$Na2SO4£Øaq£©+H2O£Øl£©”÷H=-57.3kJ/mol£»
£Ø3£©16g¹ĢĢåĮņĶźČ«Č¼ÉÕŹ±·Å³ö148.4kJµÄČČĮ棬¼“1molSĶźČ«Č¼ÉÕŹ±·Å³ö·Å³ö296.8kjČČĮ棬ŌņČČ»Æѧ·½³ĢŹ½ĪŖ£ŗS£Øs£©+O2£Øg£©=SO2£Øg£©£»”÷H=-296.8 kJ/mol£¬
¹Ź“š°øĪŖ£ŗS£Øs£©+O2£Øg£©=SO2£Øg£©£»”÷H=-296.8 kJ/mol£»
£Ø4£©ŅŃÖŖ£ŗN2£Øg£©+2O2£Øg£©ØT2NO2£Øg£©”÷H=+67.7kJ/mol ¢Ł
N2H4£Øg£©+O2£Øg£©ØTN2£Øg£©+2H2O£Øg£©”÷H=-534kJ/mol ¢Ś
¢Ł¢ŚĮŖĮ¢£¬2”Į¢Ś-¢ŁµĆµ½2N2H4£Øg£©+2NO2£Øg£©ØT3N2£Øg£©+4H2O£Øg£©”÷H=2”Į¢Ś-¢Ł=2”Į£Ø-534kJ/mol£©-£Ø+67.7kJ/mol£©=-1135.7kJ/mol£¬
A£®·“Ó¦ÖŠNO2Éś³ÉN2£¬NŌŖĖŲ»ÆŗĻ¼Ū½µµĶ£¬±»»¹Ō£¬ĪŖŃõ»Æ¼Į£¬¹ŹAÕżČ·£»
B£®·“Ó¦µÄ·½³ĢŹ½ĪŖ2N2H4£Øg£©+2NO2£Øg£©ØT3N2£Øg£©+4H2O£Øg£©£¬Ö»ÓŠNŌŖĖŲ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬µŖĘų¼ČŹĒŃõ»Æ²śĪļÓÖŹĒ»¹Ō²śĪļ£¬¹ŹBÕżČ·£»
C£®ÓÉ·½³ĢŹ½æÉÖŖ2molNO2²Ī¼Ó·“Ó¦£¬Éś³É3molN2£¬×ŖŅʵē×ÓĪļÖŹµÄĮæĪŖ2”Į4mol=8mol£¬ŌņÉś³É1molN2£¬×ŖŅĘ$\frac{8}{3}$molµē×Ó£¬¹ŹC“ķĪó£»
D£®ÓÉŅŌÉĻ·ÖĪöæÉÖŖøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ2N2H4£Øg£©+2NO2£Øg£©ØT3N2£Øg£©+4H2O£Øg£©”÷H=-1135.7 kJ•mol-1£¬¹ŹD“ķĪó£»
¹Ź“š°øĪŖ£ŗCD£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éÖŠŗĶČČ”¢øĒĖ¹¶ØĀÉŅŌ¼°ČČ»Æѧ·½³ĢŹ½µÄŹéŠ“ĪŹĢā£¬±¾ĢāÄѶČÖŠµČ£¬×¢Ņā×¼Č·Ąķ½āÖŠŗĶČČŗĶČ¼ÉÕČȵÄøÅÄī£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬11.2LŃõĘųŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖNA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬1.06g Na2CO3ŗ¬ÓŠµÄNa+Ąė×ÓŹżĪŖ0.02 NA | |
| C£® | ŌŚ±ź×¼×“æöĻĀ£¬22.4 LĖ®µÄÖŹĮæŌ¼ĪŖ18g | |
| D£® | ĪļÖŹµÄĮæÅضČĪŖ0.5mol/LµÄMgCl2ČÜŅŗÖŠ£¬ŗ¬ÓŠCl-øöŹżĪŖ NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6.8 gČŪČŚµÄKHSO4ÖŠŗ¬ÓŠ0.05NAøöŃōĄė×Ó | |
| B£® | 1.0 L 2 mol/LµÄNaOH£Øaq£©ÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżÄæĪŖ2NA | |
| C£® | ŌŚ24 g18O2ÖŠŗ¬ÓŠ1.5NAøöŃõŌ×Ó | |
| D£® | ŌŚ·“Ó¦KIO3+6HI=KI+3I2+3H2OÖŠ£¬ĆæÉś³É3 mol I2×ŖŅʵĵē×ÓŹżĪŖ6NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol H2Oŗ¬ÓŠµÄŌ×ÓŹżĪŖNA | |
| B£® | 4g H2ŗ¬ÓŠĒā·Ö×ÓŹż4NA | |
| C£® | 1L 0.1 mol•L-1NaClČÜŅŗÖŠŗ¬Na+Źż0.1NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬11.2L O2ÖŠŗ¬ÓŠ·Ö×ÓŹżĪŖ0.5NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żŃõ»ÆÄĘ | B£® | µā»ÆĒā | C£® | æĮŠŌÄĘ | D£® | ĀČ»Æ¼Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
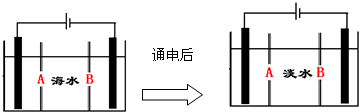
| A£® | æɵē½āČŪČŚMgCl2Ą“ÖĘČ”½šŹōĆ¾£¬Ņ²Äܵē½āČŪČŚHClĄ“ÖĘČ”Cl2 | |
| B£® | Ā±×åŌŖĖŲµÄµ„ÖŹ“ÓF2µ½I2µÄČŪµćÖš½„Éżøߣ¬Ōņ¼ī½šŹōŌŖĖŲµ„ÖŹ“ÓLiµ½CsµÄČŪµćŅ²Öš½„Éżøß | |
| C£® | µŚ2ÖÜĘŚŌŖĖŲĒā»ÆĪļĪČ¶ØŠŌĖ³ŠņŹĒHF£¾H2O£¾NH3£¬ŌņµŚČżÖÜĘŚŌŖĖŲĒā»ÆĪļĪČ¶ØŠŌĖ³ŠņŹĒHCl£¾H2S£¾PH3 | |
| D£® | ÉŁĮæµÄCl2ĶØČėFeBr2ČÜŅŗÖŠÉś³ÉFeCl3ŗĶFeBr3£¬ŌņÉŁĮæµÄCl2ĶØČėFeI2 ČÜŅŗÖŠŅ²Éś³ÉFeCl3ŗĶFeI3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³żČ„KClÖŠ»ģÓŠµÄKI£ŗČÜÓŚĖ®ĶØČė¹żĮæĀČĘų£¬Õō·¢½į¾§ | |
| B£® | ³żČ„BaSO4¹ĢĢåÖŠ»ģÓŠµÄBaCO3£ŗ¼Ó¹żĮæŃĪĖįŗ󣬹żĀĖ | |
| C£® | ³żČ„Na2CO3¹ĢĢåÖŠµÄNaHCO3£ŗ¼ÓČČÖĮŗćÖŲ | |
| D£® | ³żČ„CuOÖŠ»ģÓŠµÄAl2O3£ŗ¼Ó¹żĮæŃĪĖįŗ󣬹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com