
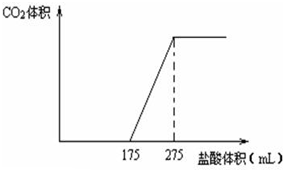
 取NaHCO3和Na2O2的固体混合物x g放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如下图所示.试回答下列问题:
取NaHCO3和Na2O2的固体混合物x g放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如下图所示.试回答下列问题:
| ||
| 3.94g |
| 197g/mol |
| 0.02mol |
| (275-175)×10-3L |
| 0.2mol/L×275ml×10-3L/ml×2-0.04mol |
| 2 |
| ||


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
| A、向Fe(OH)3胶体中滴加稀硫酸,先生成红褐色沉淀,后沉淀逐渐溶解 |
| B、向铜粉中加入稀硫酸,铜粉不溶解,再加入硝酸钾固体,铜粉逐渐溶解 |
| C、向明矾(KAl(SO4)2?12H2O)溶液中滴入Ba(OH)2溶液,SO42-恰好完全沉淀时的离子方程式为:Ba2++3OH-+Al3++SO42-═BaSO4↓+Al(OH)3↓ |
| D、氯碱工业和金属钠的冶炼都用到了NaCl,阳极上发生的电极反应都是:2Cl-+2e-=Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| B、用热的纯碱溶液可以更好地去除油污 |
| C、pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
| D、在pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,由水电离的c (H+) 后者大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
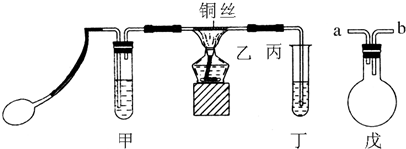
 为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验.
为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com