
【题目】某溶液中可能含有![]() 、OH-、
、OH-、![]() 、
、![]() 、[Al(OH)4] -、
、[Al(OH)4] -、![]() 、Na+、Mg2+、Fe3+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示。下列说法正确的是
、Na+、Mg2+、Fe3+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示。下列说法正确的是
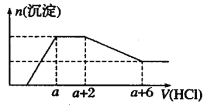
A.原溶液中一定含有Na2SO4
B.原溶液中含有![]() 与[Al(OH)4] -的物质的量之比为1 :2
与[Al(OH)4] -的物质的量之比为1 :2
C.反应最后形成的溶液中的溶质只有NaCl
D.原溶液中一定含有的阴离子是OH-、![]() 、
、![]() 、[Al(OH)4] -
、[Al(OH)4] -
【答案】D
【解析】
根据图象曲线变化可知,开始无沉淀生成说明加入的盐酸和溶液中的碱反应,说明溶液中一定含氢氧根离子,则与氢氧根离子不能共存的有Mg2+、Fe3+、Al3+,随后反应生成沉淀逐渐增大,说明是[Al(OH)4] -和氢离子反应生成氢氧化铝沉淀和硅酸沉淀,由于[Al(OH)4] -与![]() 发生反应生成氢氧化铝沉淀,则溶液中一定不存在
发生反应生成氢氧化铝沉淀,则溶液中一定不存在![]() ,继续加入盐酸沉淀量不变,消耗盐酸的离子只能是
,继续加入盐酸沉淀量不变,消耗盐酸的离子只能是![]() 离子,反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐
离子,反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐
酸,最后剩余沉淀为硅酸;硫酸根离子不能确定存在,但根据溶液的电中性可知,溶液中一定含有钠离子离子,据此进行解答。
根据图象曲线变化可知,开始无沉淀生成说明加入的盐酸和溶液中的碱反应,说明溶液中一定含氢氧根离子,则与氢氧根离子不能共存的有Mg2+、Fe3+、Al3+,随后反应生成沉淀逐渐增大,说明是[Al(OH)4] -和氢离子反应生成氢氧化铝沉淀和硅酸沉淀,由于[Al(OH)4] -与![]() 发生反应生成氢氧化铝沉淀,则溶液中一定不存在
发生反应生成氢氧化铝沉淀,则溶液中一定不存在![]() ,继续加入盐酸沉淀量不变,消耗盐酸的离子只能是
,继续加入盐酸沉淀量不变,消耗盐酸的离子只能是![]() 离子,反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐
离子,反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐
酸,最后剩余沉淀为硅酸;硫酸根离子不能确定存在,但根据溶液的电中性可知,溶液中一定含有钠离子。
A、溶液中硫酸根离子不能确定,剩余原溶液不中一定含有Na2SO4,故A错误;
B、依据图象可知和碳酸根离子反应的盐酸为2体积,![]() +2H+=CO2↑+H2O,氢氧化铝溶解消耗的盐酸体积为4体积,Al(OH)3+3H+=Al3++3H2O,原溶液中含有
+2H+=CO2↑+H2O,氢氧化铝溶解消耗的盐酸体积为4体积,Al(OH)3+3H+=Al3++3H2O,原溶液中含有![]() 与[Al(OH)4] -的物质的量之比为3: 4,故B错误;
与[Al(OH)4] -的物质的量之比为3: 4,故B错误;
C、反应最后形成的溶液中的溶质为NaCl和AlCl3,故C错误;
D、依据判断原溶液中一定含有的阴离子是:OH-、![]() 、
、![]() 、[Al(OH)4] -,故D正确;
、[Al(OH)4] -,故D正确;
故选D。


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
【题目】已知:①C(s、金刚石) + O2(g)=CO2(g) ΔH1=-395.4 kJmol-1,② C(s、石墨) + O2(g)=CO2(g) ΔH2=-393.5 kJmol-1 上述反应中的能量变化如图所示,下列说法正确的是

A.石墨和金刚石之间的转化是物理变化
B.图中 b 代表反应①的能量变化
C.C(s、金刚石) =C(s、石墨) ΔH= +1.9 kJmol-1
D.金刚石比石墨的热稳定性好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示:
Ⅰ.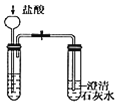 Ⅱ.
Ⅱ. 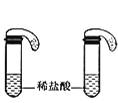 Ⅲ.
Ⅲ. 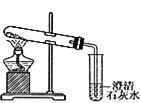 Ⅳ.
Ⅳ. 
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的是(填装置序号)___________;
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其加热时都能发生的反应的化学方程式为_________.
(3)有同学认为,除上述试验方法外,向两种固体配成的溶液中加入澄清石灰水也可以区分它们,这种说法是________(填“正确”或“错误”)的.其中向NaHCO3溶液中加入足量澄清石灰水,发生反应的离子方程式为:______
(4)另有两瓶溶液,已知分别是K2CO3溶液和NaHCO3溶液,请你写出鉴别方法_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应。请回答下列问题:
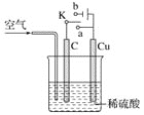
(1)甲同学认为,不通入空气,将 K 与_____(填“a”或“b”)连接,即可实现。则总反应的离子方程式为_____。
(2)乙同学认为在通入空气的同时,将开关 K 与_____连通,也可以实现,则电池总反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置:
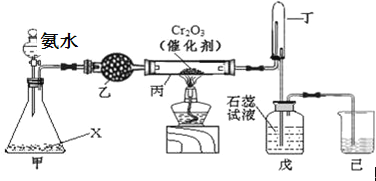
(1)若分液漏斗中氨水的浓度为9.0molL﹣1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、玻璃棒、 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X的名称为 。
(3)乙装置的作用是 ;写出受热时丙装置发生反应的化学方程式为 。
(4)当戊中观察到 现象,则说明已制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因 。如何改进置 。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下在2L密闭容器中加人一定量A,发生以下化学反应:2A(g)![]() B(g)+C(g) ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是
B(g)+C(g) ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是
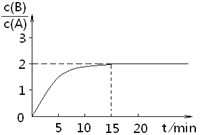
A.反应达平衡时,A的转化率为80%
B.A的初始物质的量为4mol
C.反应到达平衡时,放出的热量是193kJ
D.15min时,v正= v逆=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“温室效应”是哥本哈根世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
(1)下列措施中,有利于降低大气中CO2浓度的是__________(填字母编号)。
A 采用节能技术,减少化石燃料的用量
B 鼓励乘坐公交车出行,倡导“低碳”生活
C 利用太阳能、风能等新型能源替代化石燃料
(2)CH4是另一种主要的温室气体,lg甲烷完全燃烧生成液态水和二氧化碳,放出55.64kJ的热量,写出表示甲烷燃烧的热化学方程式_______________。
(3)酸雨的形成主要是由废气中的SOx和NOx造成的,某空气污染监测仪是根据SO2与Br2、H2O的定量反应来测定空气中SO2含量的,该反应的化学方程式为:____________。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。第一阶段燃烧黄铁矿的化学方程式为4FeS2+11O2![]() 2Fe2O3+8SO2:第二阶段的反应原理是2SO2(g)+O2(g)
2Fe2O3+8SO2:第二阶段的反应原理是2SO2(g)+O2(g)![]() 2SO3(g),其生产设备的名称为接触室;在生产过程中某一时刻取样SO2、O2、SO3的浓度分别为2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是__________(填字母编号)
2SO3(g),其生产设备的名称为接触室;在生产过程中某一时刻取样SO2、O2、SO3的浓度分别为2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是__________(填字母编号)
A SO2为5mol·L-1,O2为3.5mol·L-1
B SO2为3mol·L-1
C SO2、SO3均为2.5mol·L-1
D SO3为5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色的混合气体甲中可能含有NO2、NO、CO2、O2、NH3、N2中的几种,将100mL甲气体经过如图所示的实验装置进行处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为(不考虑Na2O2与NO2、NO的反应)( )

A.NO2、CO2、N2B.NH3、NO、CO2
C.NH3、N2、CO2D.NO、O2、NH3
【答案】B
【解析】
该气体无色,说明其中不含NO2;气体通过浓硫酸体积减小,说明其中有NH3;气体通过足量Na2O2后显红棕色,说明其中含有CO2和NO,故不含O2;最后通入水中无气体剩余,说明其中不存在N2,选项B正确,故答案为B。
【题型】单选题
【结束】
19
【题目】A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色。有关的转化关系如图所示(反应条件与部分反应的生成物略去)。

请回答下列问题:
(1)D的化学式为__,Y的化学式为__,E的化学式为__。
(2)Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为__。
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为__。
(4)气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),洗气瓶中是否有沉淀生成?__,理由是__。
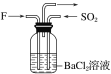
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法错误的是( )
A.室温下44gCO2含有的分子数是NA
B.常温下,46gNO2和N2O4的混合气体中含有的氮原子数目为NA
C.常温下,22.4LH2O含有10NA个电子
D.若120g石墨能写a个字,则平均每个字约含有![]() 个碳原子
个碳原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com