
向某晶体的水溶液中加入FeCl2的溶液后,无明显变化,当滴加几滴溴水后,混合液出现血红色。那么,由此得出的下列结论错误的是( )21教育名师原创作品
A.该晶体中一定含有SCN-
B.Fe3+与SCN-形成了血红色Fe(SCN)3难溶物
C.Fe2+被Br2氧化为Fe3+
D.Fe2+与SCN-不能形成血红色物质
科目:高中化学 来源: 题型:
右图为一原电池的结构示意图,下列说法中,错误的是
A.Cu电极为正极
B.原电池工作时,电子从Zn电极流出
C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu
D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应。二者比较,相等的是( )www.21-cn-jy.com
①铜片消耗完所需时间 ②反应生成的气体体积(标准状况) ③反应中氧化剂得到的电子总数 ④反应后溶液中铜离子的浓度
A.①③ B.②④
C.③④ D.只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
Ⅰ.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
Ⅱ.向Ⅰ所得固体中加入过量稀H2SO4,充分反应后过滤;
Ⅲ.向Ⅱ所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
Ⅳ.……
(1)步骤Ⅰ中发生反应的化学方程式为________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)步骤Ⅱ所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+。用离子方程式解释其可能的原因________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)步骤Ⅲ获得CuSO4溶液的离子方程式为________________________________________________________________________
________________________________________________________________________。
(4)步骤Ⅱ所得滤液经进一步处理可制得Na2FeO4,流程如下:



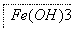


①测得滤液中c(Fe2+)为a mol·L-1,若要处理滤液,理论上需要消耗25%的H2O2溶液 68a kg(用含a的代数式表示)。2-1-c-n-j-y
②写出由Fe(OH)3制取Na2FeO4的化学方程式 2Fe(OH)3+3NaClO+4NaOH 2Na2FeO4+3NaCl+5H2O 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物。(反应条件图中已省略)
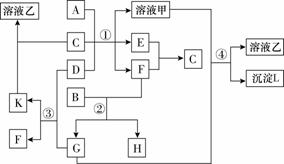
(1)A、B、C、D代表的物质分别为______、______、______、______(填化学式);
(2)反应①中的C、D均过量,该反应的化学方程式是
________________________________________________________________________
________________________________________________________________________;
(3)反应②中,若B与F物质的量之比为4∶3,G、H分别是 CO2 、 CO (填化学式);
(4)反应③产物中K的化学式为 Na2CO3 ;
(5)反应④的离子方程式为________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:
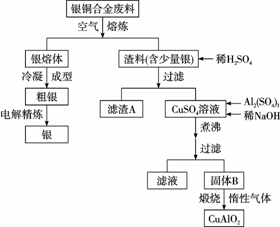
[注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃]
(1)电解精炼银时,阴极反应式为 Ag++e- Ag ;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 2NO+O2 2NO2 。
(2)固体混合物B的组成为 Al(OH)3和CuO ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 Al(OH)3+OH- AlO +2H2O 。2·1·c·n·j·y
+2H2O 。2·1·c·n·j·y
(3)完成煅烧过程中一个反应的化学方程式:
4 CuO+ 2 Al2O3 4 CuAlO2+ O2 ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0 kg废料中的铜可完全转化为 50 mol CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液 25.0 L。www.21-cn-jy.com
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 蒸发浓缩、冷却结晶 、过滤、洗涤和干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属及其化合物的说法正确的是( )
A.1 L生理盐水(0.9%NaCl溶液)中含有9 mol Na+
B.出土的古代铜制品表面覆盖着铜绿,其主要成分是CuO
C.装修门窗使用的铝合金材料的硬度比铝小,熔点比铝低
D.节日燃放的烟花是某些金属元素发生焰色反应所呈现出来的色彩
查看答案和解析>>
科目:高中化学 来源: 题型:
用水稀释0.1 mol/L氨水时,溶液中随水量的增加而减小的是
A.c(OH-)/c(NH3·H2O) B.c(NH3·H2O)/c(OH-)
C.c(H+)和c(OH-)的乘积 D.n(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com