
⑴室温时,pH=a的氨水与PH =b的盐酸等体积混合,恰好完全反应,则氨水电离度可表示为_______________ (用百分数来表示)
(2)室温下,0.1 mol/LNaClO溶液的pH_________0.1 mol/LNa2SO3溶液的pH。(选填“大于”、“小于”,或“等于”)。浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为 。
已知:
H2SO3 | Kal=1.54×l0-2 | Ka2=1.02×10-7 |
HCIO | Ka1=2.95×10-8 | |
H2CO3 | Kal=4.3×10-7 | Ka2=5.6×10-11 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届黑龙江牡丹江第一高级中学高三12月月考化学卷(解析版) 题型:选择题
甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是
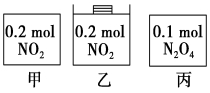
A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙
B.平衡时N2O4的百分含量:乙>甲=丙
C.平衡时甲中NO2与丙中N2O4的转化率相同
D.平衡时混合物的平均相对分子质量:甲>乙>丙
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:推断题
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3) 2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀.
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体.
(3)取滤液做焰色反应,可证明滤液中含Na +,不含K +.
由上述现象推断:
(1)该混合物中一定含有_________;一定不含有_________,可能含有_________.
(2)如要检验其是否存在,将如何操作_________.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 配制一定浓度的稀硫酸,用量筒量取浓硫酸后,未将蒸馏水洗涤量筒后的洗涤液转移至容瓶中,使配制的溶液浓度偏小
B. pH试纸使用时不需要润湿,红色石蕊试纸检测气体时也不需要润湿
C. 蒸发时将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热
D. 蒸馏实验中,忘记加沸石,可以先停止加热,待溶液冷却后加入沸石,再继续加热蒸馏
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A.钠是一种强还原剂,可以将钛、铌等金属从其氯化物溶液中置换出来
B.铜能与氯化铁溶液反应,该反应可以应用于印刷电路板的制作
C.人们发现了118种元素,即共有118种核素
D.H2和D2互为同位素
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
下列有关电解质溶液中微粒的物质的量的浓度关系正确的是
A.在0.1mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1mol·L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H2CO3)+ c(H+)
C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1mol·L-1NaOH溶液:
c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol·L-1]:
c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
某温度下,在固定容积的容器中,可逆反应A(g)+3B(g)  2C(g)达到平衡时,各物质的物质的量之比为n(A) : n(B): n(C)=2 : 2 : 1••保持温度不变,以2 : 2 : 1的物质的量之比再充入A、B、C,则
2C(g)达到平衡时,各物质的物质的量之比为n(A) : n(B): n(C)=2 : 2 : 1••保持温度不变,以2 : 2 : 1的物质的量之比再充入A、B、C,则
A.平衡不移动
B.再达平衡时,n(A) : n(B) : n(C)仍为2 : 2 : 1
C.再达平衡时,C的体积分数增大
D.再达平衡时,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源:2017届安徽师大附中高三上新课标模拟化学卷(解析版) 题型:填空题
合成氨是最重要的化工生产之一,回答下列问题:
I.氢气通常用生产水煤气的方法制得。其中CO(g)+H2O(g)  CO2(g) + H2(g) △H<0,在 850℃时,平衡常数 K=1。
CO2(g) + H2(g) △H<0,在 850℃时,平衡常数 K=1。
(1)若升高温度到950℃时,达到平衡时K_________1(填“>”“<”或“ = ”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO、3.0mol H2O、1.0mol CO2和xrnolH2,则:
①当x= 5.0时,上述平衡向_________(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是_____________。
(3)在850℃时,若设x=5.0mol和x= 6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a_______b(填“大于”、“小于”或“等于”)。
II.氨和尿素【CO(NH2)2】溶液都可以吸收硝酸工业尾气中的NO、NO2,将其转化为N2。
(4)尿素与NO、NO2三者等物质的最反应为:CO(NH2)2+NO+NO2=CO2+2N2+2H2O
该反应中的氧化剂为________(写化学式)。
若反应生成标况下N2 33.6L,则转移电子的数目为___________。
(5)已知:N2(g)+O2(g)=2NO(g)△H1=akJ ·mol-1
N2(g)+3H2(g) = 2NH3(g) △H2 = bkJ • mol-1
2H2(g) +O2(g) = 2H2O(g) △H3=ckJ • mol-1
则4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g) △H=__________。
III.(6)合成氨盐也是氨的重要用途,测定其中的含氮量可以采用“甲醛法”。即4NH4++6HCHO (CH2)6N4+4H++6H2O。 现有一种纯净的铵盐,可能是硝酸铵、硫酸铵或碳酸铵中的一种。称取2g该铵盐溶于水,加入足量的甲醛溶液后,再加人水配成100mL溶液,取出10mL,滴入酚酞后再逐滴滴入0.lmol/L的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色,则该铵盐中氮的质量分数是_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:选择题
某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol/L的盐酸,测得溶液中CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

A.a曲线表示的离子方程式为AlO2-+H++H2O==Al(OH)3↓
B.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
C.V1∶V2=l∶5
D.M点时生成的CO2为0.05 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com