
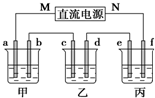
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:分析 (1)接通电源,经过一段时间后,乙中c电极质量增加,说明c是银离子放电生成单质银,所以c是阴极,则M是负极,则N是正极;
(2)电极d是阳极,电极上发生的电极反应式为4OH--4e-═2H2O+O2↑;
(3)甲池为电解饱和食盐水,总反应式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;
(4)当电路中有0.04mol电子通过时,a是氢离子放电,生成氢气,b是氯离子放电生成氯气、c极是银离子放电生成单质银、d电极是氢氧根离子放电生成氧气,所以有0.04mol电子通过时产生的气体或固体的物质的量分别是0.02mol、0.02mol、0.04mol、0.01mol;
(5)若利用丙池实现铁上镀铜,所以e阴极是铁,f阳极是铜,电解质溶液是硫酸铜,若利用丙池实现电解精炼铜,e阴极是纯铜,f阳极是粗铜,电解质溶液是硫酸铜,由此分析解答.
解答 解:(1)接通电源,经过一段时间后,乙中c电极质量增加,说明c是银离子放电生成单质银,所以c是阴极,则M是负极,则N是正极,故答案为:正;
(2)电极d是阳极,电极上发生的电极反应式为4OH--4e-═2H2O+O2↑,故答案为:4OH--4e-═2H2O+O2↑;
(3)甲池为电解饱和食盐水,总反应式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;
(4)当电路中有0.04mol电子通过时,a是氢离子放电,生成氢气,b是氯离子放电生成氯气、c极是银离子放电生成单质银、d电极是氢氧根离子放电生成氧气,所以有0.04mol电子通过时产生的气体或固体的物质的量分别是0.02mol、0.02mol、0.04mol、0.01mol,所以a、b、c、d电极上产生的气体或固体的物质的量之比是2:2:4:1,故答案为:2:2:4:1;
(5)若利用丙池实现铁上镀铜,所以e阴极是铁,f阳极是铜,电解质溶液是硫酸铜,若利用丙池实现电解精炼铜,e阴极是纯铜,f阳极是粗铜,电解质溶液是硫酸铜,故答案为:Fe-Cu-CuSO4;纯铜-粗铜-CuSO4.
点评 本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意三个电解池为串联电路,各电极上得失电子的数目相等,做题时要正确写出电极方程式,准确判断两极上离子的放电顺序.


科目:高中化学 来源: 题型:多选题
| A. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,则该溶液一定是钠盐溶液 | |
| B. | 测定同温同浓度的Na2CO3和Na2SiO3溶液的pH,发现Na2SiO3溶液的pH大,则碳的非金属性强于硅 | |
| C. | 淀粉与稀硫酸混合加热一段时间,滴加银氨溶液并水浴加热,无银镜出现,则淀粉没有水解 | |
| D. | 向浓度均为0.1 mol•L-1 NaCl和NaI混合溶液中滴加少量稀AgNO3溶液,出现黄色沉淀,说明Ksp(AgCl)>Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热时间太短 | B. | 不应冷却后再加入AgNO3 | ||
| C. | 加AgNO3溶液前未用稀HNO3酸化 | D. | 反应后的溶液中不存在Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片作正极 | B. | 正极反应为:2H++2e-═H2↑ | ||
| C. | 溶液中的H+移向正极 | D. | 锌片作负极,锌发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 图为实验室制取某有机物的装置图,试通过已学知识回答下列问题:
图为实验室制取某有机物的装置图,试通过已学知识回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
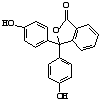
| A. | 分子式为C20H14O4 | |
| B. | 可以发生取代反应、加成反应、氧化反应 | |
| C. | 含有的官能团有羟基、酯基 | |
| D. | 1 mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值分别为10 mol 和4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①④⑤ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com