
【题目】某金属首饰可能含有铜或银,欲检验其是否用纯金制成,可把样品浸入某溶液一段时间后,取出洗净、干燥后称量,根据质量是否变化即可判断.可以选用的溶液是( )
A.稀硫酸
B.盐酸溶液
C.稀硝酸
D.氢氧化钠溶液
科目:高中化学 来源: 题型:
【题目】25℃时,某些弱酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)物质的量浓度为0.1 mol·L-1的下列四种物质:
a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,pH由大到小的顺序是________(填编号)。
(2)常温下0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是________。
A.c(H+) B. ![]()
C.c(H+)·c(OH-) D. ![]()
(3)体积为10 mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1 000 mL,稀释过程pH变化如图。则HX的电离平衡常数__________(填“大于”、“等于”或“小于”)醋酸的平衡常数,理由是______________________________。
稀释后,HX溶液中水电离出来的c(H+)________(填“大于”、“等于”或“小于”)醋酸溶液中水电离出来的c(H+),理由是_____________________________________。

(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=________(填准确数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月9日发布了113号Nh、115号Mc、117号Ts、118号Og这4种新元素的中文名称,分别为![]() 、“镆”(mò)、
、“镆”(mò)、 ![]() (tián)、
(tián)、 ![]() (ào)。下列有关说法正确的是
(ào)。下列有关说法正确的是
A. 115号元素在周期表中的位置是第七周期VB
B. 这四种元素都是主族元素
C. 118号元素在通常情况下呈气态,其余三种为固态
D. 117号元素Ts位于金属非金属分界线上,可能是半导体,与它同族的上一周期元素的原子序数为99
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素在化学反应中由化合态变为游离态,则该元素( )
A.一定被还原了 B.一定被氧化了
C.既可能被氧化也可能被还原 D.既不可能被氧化,也不可能被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由黄铜矿(主要成分CuFeS2,质量分数为90%)冶炼铜的主要流程如下:

己知:一定条件下,铝可以和某些金属氧化物反应置换金属
(1)高温焙烧前要将黄铜矿粉碎的目的是_________________。
(2)气体A中的大气污染物可选用下列试剂中的____________吸收。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(3)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在____(填离子符号),欲检验溶液中还存在Fe2+,所需试剂是_________。
(4)由泡铜冶炼粗铜的化学反应方程式为_________。
(5)某同学用铜、稀硫酸和H2O2制备CuSO4溶液,其化学反应方程式为_________,反应停止后除去溶液中过量的H2O2的简便方法是_____________。
(6)1.15吨该黄铜矿理论上可以得到含杂质10%的粗铜质量为_________kg(冶炼过程中铜损失忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组制备氢氧化亚铁沉淀。
实验1 |
| 实验现象 |
液面上方产生白色絮状沉淀,迅速变为灰绿色,振荡,试管壁上有红褐色沉淀生成。 |
(1)实验1中产生白色沉淀的离子方程式是________________。
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究:
① 甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物。查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有 Fe(OH)3,方案是__________。
② 乙同学查阅文献:Fe(OH)2在大量SO42存在的情况下形成Fe6(SO4)2(OH)4O3(一种氧基碱式复盐)。并设计对比实验证实该假设:向试管中加入_____________,再往试管中加入____________,振荡,现象与实验1相同,结论是该假设不成立。
③ 乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起。推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好。设计了如下实验方案:
试管中10 mL NaOH溶液 | 滴加 FeSO4溶液 | 实验现象 | |
实验2 | 6 mol/L NaOH溶液 | 0.2mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有少量灰绿色) ,沉淀下沉后,大部分灰绿色变为白色沉淀 |
实验3 | 6 mol/L NaOH溶液 | 0.1mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有极少量灰绿色) ,沉淀下沉后,底部都为白色沉淀 |
该实验得出的结论是_______________,能说明灰绿色是由Fe(OH)2表面吸附Fe2+引起的证据是____________。丙同学认为该实验方案不足以证明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,还需补充的实验是________________,证明该假设成立。
(3)丙同学探究温度对氢氧化亚铁制备实验的影响:取少量灰绿色沉淀,在水浴中加热,颜色由灰绿变白,且有絮状白色沉淀下沉,原因为_____________。
(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解气用途广泛,由石油裂解气合成生物可降解高聚物J的合成线路如下:
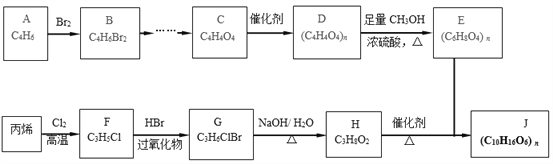
已知:
i.酯与酯可发生如下酯交换反应:RCOOR'+R"OH![]() RCOOR"+R'OH(R、R'、R"代表烃基)
RCOOR"+R'OH(R、R'、R"代表烃基)
ii.烯烃中,碳碳双键相邻为不稳定结构,碳碳双键易被氧化剂氧化。
(1)A为链状烃,其核磁共振氢谱中有两组峰且面积之比是1:2,则A的名称为____________。
(2)B 中所含官能团名称为____________ 。
(3)C→D的反应类型 ______________。
(4)C能与足量的 NaHCO3 溶液反应生成C4H2O4Na2, C的结构简式为_______________。
(5)D→E的化学方程式是 ______________。
(6)H中不含甲基,H与E形成对称型高聚物J的化学方程式是______________。
(7)请完成 B → C 的合理路线________________ 。( 无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能。下表是某些共价键的键能:根据右图中能量变化图,回答下列问题:
(1)图中:a=___________。

(2)表格中:X=__________。
共价键 | H-H | O=O | H-O |
键能/kJ ·mol-1 | 436 | 498 | X |
Ⅱ.如图,A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________。
(3)C中被腐蚀的金属是________,总反应的化学方程式为_________________________,
比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为__________(填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com