
判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示:
含氧酸酸性强弱与非羟基氧原子数的关系
| 次氯酸 | 磷酸 | 高氯酸 | |
| 含氧酸 | Cl-OH |
|
|
| 非羟基氧原子数 | 0 | 1 | 3 |
| 酸性 | 弱酸 | 中强酸 | 最强酸 |
(1)亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构简式分别为①________________,②________________。
(2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
①________________________________________________________________________,
②________________________________________________________________________。
(3)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况:________________________________________________________________________,
写出化学方程式:_____________________________________________________。
答案 (1)①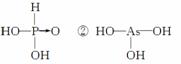
(2)①H3PO3+2NaOH===Na2HPO3+2H2O
②H3AsO3+3NaOH===Na3AsO3+3H2O
(3)H3PO3为中强酸,不与盐酸反应,H3AsO3可与盐酸反应 H3AsO3+3HCl===AsCl3+3H2O
解析 此题属于无机含氧酸的结构、性质推断题,考查同学们运用题给信息推断物质结构和性质的能力。(1)已知H3PO3为中强酸,H3AsO3为弱酸,依据题给信息可知H3PO3中含1个非羟基氧原子,H3AsO3中不含非羟基氧原子。(2)与过量NaOH溶液反应的化学方程式的书写,需得知H3PO3和H3AsO3分别为几元酸,从题给信息可知,含氧酸分子结构中含几个羟基氢,则该酸为几元酸。故H3PO3为二元酸,H3AsO3为三元酸。(3)H3PO3为中强酸,不与盐酸反应;H3AsO3为两性物质,可与盐酸反应。


科目:高中化学 来源: 题型:
具有下列电子构型的原子中,第二电离能与第一电离能差值最大的是( )
A.1s22s22p5 B.1s22s22p6
C.1s22s22p63s1 D.1s22s22p63s2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除杂方法正确的是( )
①除去乙烷中少量的乙烯:通入H2,加催化剂反应
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液
③除去NaBr溶液中的NaI:用氯水氧化NaI,再用CCl4萃取分液
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤只含有泥沙的粗盐:可通过溶解、过滤、蒸发、结晶的方法提纯
A.①②③ B.②④⑤ C.③④⑤ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
判断下列说法是否正确,正确的划“√”,错误的划“×”
(1)氢键是氢元素与其他元素形成的化学键( )
(2)可燃冰(CH4·8H2O)中甲烷分子与水分子间形成了氢键( )
(3)乙醇分子和水分子间只存在范德华力( )
(4)碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键( )
(5)水分子间既存在范德华力,又存在氢键( )
(6)氢键具有方向性和饱和性( )
(7)H2和O2之间存在氢键( )
(8)H2O2分子间存在氢键( )
(9)卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大( )
(10)氢键的存在一定能使物质的熔、沸点升高( )
(11)极性分子中可能含有非极性键( )
(12)H2O比H2S稳定是因为水分子间存在氢键( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.以非极性键结合起来的双原子分子一定是非极性分子
B.以极性键结合起来的分子一定是极性分子
C.非极性分子只能是双原子单质分子
D.非极性分子中,一定含有非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是______________________________________。
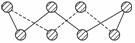
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物,则NH3分子的空间构型是________;N2H4分子中氮原子轨道的杂化类型是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
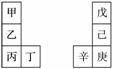
A.金属性:甲>乙>丁
B.原子半径:辛>己>戊
C.丙与庚的原子核外电子数相差11
D.乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com