
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )
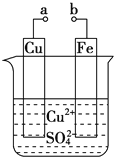
A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D. a和b用导线连接时,Fe片上发生还原反应,溶液中SO42-向铜电极移动
【答案】D
【解析】分析:a和b不连接时,不能构成原电池,铁与硫酸铜发生置换反应生成硫酸亚铁和铜;a和b用导线连接时,构成原电池,铁是负极,铜是正极,结合选项分析判断。
详解:A.a和b不连接时,由于金属活动性Fe>Cu,所以在铁片上会发生反应:Fe+Cu2+=Fe2++Cu,在铁片有金属铜析出,A正确;
B.a和b用导线连接时,形成了原电池,Cu作原电池的正极,在铜片上发生的反应为:Cu2++2e-=Cu,B正确;
C.无论a和b是否连接,Fe都会失去电子,变为Fe2+,而Cu2+会得到电子变为Cu,所以铁片均会溶解,溶液从蓝色逐渐变成浅绿色,C正确;
D.a和b用导线连接后,铁作负极,铜作正极,铁片上发生氧化反应,溶液中硫酸根离子向铁电极移动,D错误。答案选D。


科目:高中化学 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar] , 有个未成对电子.
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键.从原子结构角度分析,原因是 .
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因 .
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | ﹣49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂.Zn、Ge、O电负性由大至小的顺序是 .
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为微粒之间存在的作用力是 .
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,如图(1、2)为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ![]() ,0,
,0, ![]() );C为(
);C为( ![]() ,
, ![]() ,0).则D原子的坐标参数为 .
,0).则D原子的坐标参数为 .
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76pm,其密度为gcm﹣3(列出计算式即可).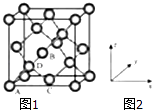
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙烯并检验乙烯性质的装置如图. 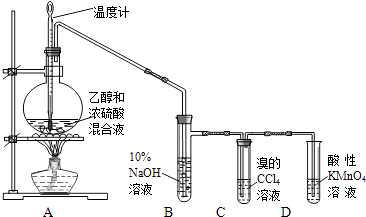
请回答有关问题:
(1)烧瓶中除反应物以外,还应放2﹣3块碎瓷片,目的是 .
(2)烧瓶中产生乙烯的反应方程式为 .
(3)反应开始后,可观察到C和D中共同的现象是;
C中的反应类型为反应、D中的反应类型为反应.
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是;10%的NaOH溶液起的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mol两种气态烃组成的混合气体完全燃烧后,将得到产物依次通入浓硫酸和石灰水中,其中浓硫酸质量增加了36g,并生成了150g沉淀.下列说法正确的是( )
A.一定有乙烷
B.一定有甲烷
C.一定没有甲烷
D.不一定有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如图.下列有关说法中正确的是( ) 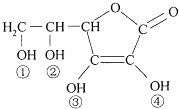
A.维生素C由于含有C═O键而能发生银镜反应
B.维生素C由于含有酯基而难溶于水
C.维生素C的分子式为C6H8O6
D.维生素C的酸性可能是①、②两个羟基引起的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧化学键断裂和新化学键形成的过程。化学键的键能是指拆开(或形成)1 mol某化学键所吸收(或放出)的能量。已知白磷(P4)和P4O6的分子结构如图所示,现提供以下化学键的键能:P—P为198 kJ/mol,P—O为360 kJ/mol,氧气分子内氧原子间的键能为498 kJ/mol,则P4(s)+3O2(g)===P4O6(s)的反应热ΔH为( )

A. +1 638 kJ/mol B. -1 638 kJ/mol
C. -126 kJ/mol D. +126 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)已知下列两个热化学方程式: C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=﹣2220.0kJmol﹣1
H2O(l)=H2O(g)△H=+44.0kJmol﹣1则0.5mol C3H8燃烧生成CO2和气态水时释放的热量为kJ.
(2)已知:①CO(g)+ ![]() O2(g)=CO2(g)△H=﹣283.0kJmol﹣1②CH3OH(l)+
O2(g)=CO2(g)△H=﹣283.0kJmol﹣1②CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=﹣726.5kJmol﹣1
O2(g)=CO2(g)+2H2O(l)△H=﹣726.5kJmol﹣1
请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: .
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂1molN﹣N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为2molN2时的△H= . (填﹣724kJmol﹣1或+724kJmol﹣1) 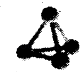
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe2+和Fe3+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是( )
A. 2∶3 B. 3∶2
C. 1∶2 D. 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的CH3COOH和NaOH溶液混合后,溶液中c(CH3COO﹣)=c(Na+),则醋酸体积氢氧化钠溶液体积(填“>”或“=”或“<”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com