
分析 (1)二氧化碳与氢气按1:4反应生成甲烷与水;
(2)水果成熟会产生乙烯,乙烯对水果具有催熟作用,且被酸性高锰酸钾氧化,据此判断;
(3)甲烷为正四面体结构,乙烯为平面型结构;
(4)丙烯具有C=C双键,具有烯烃的性质,可以发生加成反应,可以被酸性高锰酸钾氧化,与氯化氢发生加成反应,氯原子有两种不同的连接位置.
解答 解:“温室效应”是全球关注的环境问题之一,科学家们一直致力于CO2的“组合转化”技术研究.例如将CO2和H2以1:4或1:3的比例混合,在适当条件下反应,生成H2O的同时可分别获得重要的气态能源物质A和对植物生长有调节作用的有机物B,A为甲烷,B为乙烯;
(1)二氧化碳与氢气按1:4反应生成甲烷与水,方程式:CO2﹢4H2→CH4﹢2H2O;
故答案为:CO2﹢4H2→CH4﹢2H2O;
(2)II中通入乙烯,对水果具有催熟作用,最先成熟,水果成熟过程中会产生乙烯,对水果具有催熟作用,乙烯易被酸性高锰酸钾氧化,故III中产生的乙烯被氧化,成熟最慢,故成熟先后顺序为:II I III,
故答案为:II I III;
(3)甲烷为正四面体结构,乙烯为平面型结构,6个原子共面;
故答案为:正四面体;6;
(4)a.丙烯与氯化氢发生加成反应,氯原子有两种不同的连接位置,有2种产物,故a错误;
b.丙烯具有C=C双键,具可以被酸性高锰酸钾氧化,使酸性高锰酸钾溶液褪色,故b正确;
c.丙烯具有C=C双键,可以与溴发生加成反应,使溴水褪色,故c正确;
d.丙烯具有C=C双键,丙烯能发生加成反应,故d正确.
故选:a.
点评 本题考查了常见有机物的结构与性质,熟悉甲烷、乙烯分子结构及性质即可解答,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不管什么反应使用催化剂,都可以加快反应速率 | |
| B. | 可逆反应A(g)?B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大 | |
| C. | 对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大 | |
| D. | 参加反应的物质的性质是决定化学反应速率的主要因素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )| A. | BC段为Fe3+的变化曲线 | |
| B. | 原混合溶液中FeBr2的物质的量为6mol | |
| C. | 当通入2mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 海水经过加碱、加酸、浓缩结晶、过滤干燥、电解制得金属镁 | |
| B. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| D. | 金属镁着火时,可以用二氧化碳灭火器来灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 由Fe跟S直接化合可得FeS,类推出Cu跟S直接化合可得Cu2S | |
| B. | 金属镁失火不能用CO2灭火,金属钠失火也不能用CO2灭火 | |
| C. | NH4Cl、NH4I结构相似,将两种固体分别加热,分解都只生成卤化氢和氨气 | |
| D. | 原电池中通常是活泼金属做负极,不活泼金属做正极,用镁和铝与NaOH溶液构成原电池时,镁是负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用稀盐酸洗涤盛放过石灰水的试剂瓶 | |
| B. | 配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸 | |
| C. | 用待测液润洗滴定用的锥形瓶 | |
| D. | Na2CO3溶液保存在带玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
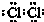 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com