
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲŹµŃé²Ł×÷µÄ½āŹĶ»ņ½įĀŪÕżČ·µÄŹĒ
Ń”Ļī | ŹµŃé²Ł×÷ | ½āŹĶ»ņ½įĀŪ |
A | Ļņŗ¬ÓŠ·ÓĢŖµÄNa2CO3ČÜŅŗÖŠ¼ÓČėÉŁĮæBaC12¹ĢĢ壬ČÜŅŗŗģÉ«±äĒ³ | Ö¤Ć÷Na2CO3ČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā |
B | ÓĆÕōĮóĖ®ČóŹŖµÄpHŹŌÖ½²āČÜŅŗpH | Ņ»¶Ø»įŹ¹²ā¶Ø½į¹ūĘ«µĶ |
C | Ļņ10mL 0.2 mol/L NaOHČÜŅŗÖŠµĪČė2µĪ0.1 mol/L MgCl2ČÜŅŗ£¬²śÉś°×É«³Įµķŗó£¬ŌŁµĪ¼Ó2µĪ0.1 mol/L FeCl3ČÜŅŗ£¬ÓÖÉś³ÉŗģŗÖÉ«³Įµķ | Ö¤Ć÷ŌŚĻąĶ¬ĪĀ¶ČĻĀµÄKsp£ŗ Mg(OH)2 £¾Fe(OH)3 |
D | ÓĆĒāŃõ»Æ¼ŲÓėÅØĮņĖį²ā¶ØÖŠŗĶ·“Ó¦µÄ·“Ó¦ČČ | ²āµĆµÄ½į¹ūĘ«Š” |
A. A B. B C. C D. D
”¾“š°ø”æA
”¾½āĪö”æNa2CO3ČÜŅŗÖŠ“ęŌŚCO32££«H2O ![]() HCO3££«OH££¬¼ÓČėÉŁĮæBaCl2£¬·¢ÉśBa2£«£«CO32£=BaCO3”ż£¬Ę½ŗāĻņÄę·“Ó¦·½Ļņ½ųŠŠ£¬c(OH£)¼õŠ”£¬ŗģÉ«±äĒ³£¬¹ŹAÕżČ·£»B”¢Čē¹ū²āµÄŹĒÖŠŠŌČÜŅŗ£¬ÓĆÕōĮóĖ®ČóŹŖµÄpHŹŌÖ½²āČÜŅŗµÄpH²»±ä£¬¹ŹB“ķĪó£»C”¢NaOHČÜŅŗÖŠ¼ÓČė¼øµĪMgCl2ČÜŅŗ£¬NaOH¹żĮ棬ŌŁ¼ÓČė¼øµĪFeCl3ČÜŅŗ£¬Fe3£«Óė¹żĮæµÄOH£·“Ӧɜ³ÉFe(OH)3³Įµķ£¬²»ÄÜĖµĆ÷ČܶȻż“󊔣¬¹ŹC“ķĪó£»D”¢ÅØĮņĖįÓėĖ®·Å³öČČĮ棬Ņņ“Ė²āµÄ·“Ó¦ČČĘ«øߣ¬¹ŹD“ķĪó”£
HCO3££«OH££¬¼ÓČėÉŁĮæBaCl2£¬·¢ÉśBa2£«£«CO32£=BaCO3”ż£¬Ę½ŗāĻņÄę·“Ó¦·½Ļņ½ųŠŠ£¬c(OH£)¼õŠ”£¬ŗģÉ«±äĒ³£¬¹ŹAÕżČ·£»B”¢Čē¹ū²āµÄŹĒÖŠŠŌČÜŅŗ£¬ÓĆÕōĮóĖ®ČóŹŖµÄpHŹŌÖ½²āČÜŅŗµÄpH²»±ä£¬¹ŹB“ķĪó£»C”¢NaOHČÜŅŗÖŠ¼ÓČė¼øµĪMgCl2ČÜŅŗ£¬NaOH¹żĮ棬ŌŁ¼ÓČė¼øµĪFeCl3ČÜŅŗ£¬Fe3£«Óė¹żĮæµÄOH£·“Ӧɜ³ÉFe(OH)3³Įµķ£¬²»ÄÜĖµĆ÷ČܶȻż“󊔣¬¹ŹC“ķĪó£»D”¢ÅØĮņĖįÓėĖ®·Å³öČČĮ棬Ņņ“Ė²āµÄ·“Ó¦ČČĘ«øߣ¬¹ŹD“ķĪó”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņFe 2 (SO 4 ) 3 ŗĶAl 2 (SO 4 ) 3 µÄ»ģŗĻČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėNaOHČÜŅŗÖĮ¹żĮ攣ĻĀĮŠĶ¼ĻóÖŠ£¬ÄÜÕżČ·±ķŹ¾ÉĻŹö·“Ó¦µÄŹĒ
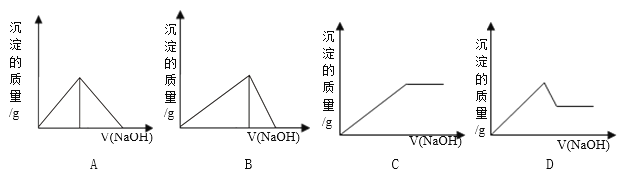
A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚĪļÖŹµÄĮæÅØ¶Č±ķŹö“ķĪóµÄŹĒ
A. ½«6.2 gŃõ»ÆÄĘČÜÓŚĖ®Åä³É1LČÜŅŗ£¬ĘäÖŠČÜÖŹµÄĪļÖŹµÄĮæÅضČĪŖ0.2mol”¤L-1
B. ½«1 L0.2 mol”¤L-1 Ca(NO3)2ČÜŅŗĻ”ŹĶµ½10 LŹ±£¬NO![]() µÄÅضČĪŖ0.04 mol”¤L-1
µÄÅضČĪŖ0.04 mol”¤L-1
C. ÓĆ1LĖ®ĪüŹÕ±ź×¼×“æöĻĀµÄ22.4L°±ĘųĖłµĆ°±Ė®ÖŠ£¬c(NH3”¤H2O)£½1mol”¤L-1
D. 5 mL2 mol”¤L-1 NaClČÜŅŗŗĶ10 mL 0.5 mol”¤L-1 MgCl2ČÜŅŗÖŠ£¬n(Cl£)ĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲW”¢X”¢Y”¢ZµÄŌ×ÓŠņŹżŅĄ“ĪŌö¼Ó£¬ÓÉÕāŠ©ŌŖĖŲ×é³ÉµÄ³£¼ūĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĻĀĶ¼£¬ĘäÖŠa”¢b”¢d”¢gĪŖ»ÆŗĻĪļ£¬aĪŖµ»ĘÉ«¹ĢĢ壬cŹĒZµÄµ„ÖŹ£¬øƵ„ÖŹÓė·ŠĖ®»ŗĀż·“Ó¦£¬ĒŅøƵ„ÖŹæÉÖĘŌģÕÕĆ÷µÆ£»fĪŖ¹ĢĢåµ„ÖŹ”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
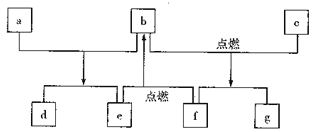
A. ¼ņµ„Ąė×ӵİė¾¶:Y>Z>X B. ŌŖĖŲµÄ·Ē½šŹōŠŌ:W>X
C. ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄ¼īŠŌ:Y>Z D. X”¢YĮ½ÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļÖ»ŗ¬Ąė×Ó¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ½«Ć¾ĀĮŗĻ½šČÜÓŚ100mLĻ”ĻõĖįÖŠ£¬²śÉś1.12LNOĘųĢå(±ź×¼×“æö)£¬Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬²śÉś³ĮµķĒéæöČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. ²»ÄÜĒó³öĻõĖįµÄĪļÖŹµÄĮæÅØ¶Č B. ĒāŃõ»ÆÄĘČÜŅŗÅضČĪŖ3mol/L
C. æÉŅŌĒó³öŗĻ½šÖŠĆ¾µÄÖŹĮæ D. æÉŅŌĒó³ö³ĮµķµÄ×ī“óÖŹĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ ( )
A. ĢśøśĻ”ĮņĖį·“Ó¦£ŗ2Fe + 6H+ ===2Fe3+ + 3H2 ”ü
B. ŃĪĖįÓė³ĪĒåŹÆ»ŅĖ®·“Ó¦£ŗH+ + OH===H2O
C. ĀČ»ÆĀĮČÜŅŗÓė¹żĮæ°±Ė®·“Ó¦£ŗAl3++3OH-=Al(OH)3”ż
D. ¶žŃõ»ÆĢ¼ĶØČė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ£ŗCO2 + OH===![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢśŌŚÉś²śÉś»īÖŠÓ¦ÓĆ×ī¹ć·ŗ£¬Į¶Ģś¼¼ŹõŗĶŗ¬ĢśŠĀ²ÄĮĻµÄÓ¦ÓƱ¶ŹÜ¹Ų×¢”£
(1)øßĀÆĮ¶ĢśŹĒŅ±Į¶ĢśµÄÖ÷ŅŖ·½·Ø£¬·¢ÉśµÄÖ÷ŅŖ·“Ó¦ÓŠ:
·“Ó¦ | ”÷H(kJ/mol) | K |
i. Fe2O3(s)+3C(s) | +489 | K1 |
ii. Fe2O3(s)+3CO(g) | X | k2 |
iii. C(s)+CO2(g) | +172 | k3 |
ŹŌ¼ĘĖć£¬X=____£¬K1”¢K2ÓėK3Ö®¼äµÄ¹ŲĻµĪŖ__________________”£
(2)T1”ꏱ£¬ĻņijŗćĪĀĆܱÕČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæµÄFe2O3ŗĶC£¬·¢Éś·“Ó¦i£¬·“Ó¦“ļµ½Ę½ŗāŗó£¬ŌŚt1Ź±æĢ£¬øıäijĢõ¼ž£¬V(Äę)Ėꏱ¼ä(t)µÄ±ä»Æ¹ŲĻµČēĶ¼1ĖłŹ¾£¬Ōņt1Ź±æĢøıäµÄĢõ¼žæÉÄÜŹĒ_______(ĢīŠ“×ÖÄø)”£
a.±£³ÖĪĀ¶Č²»±ä£¬Ń¹ĖõČŻĘ÷ b.±£³ÖĢå»ż²»±ä£¬ÉżøßĪĀ¶Č
c.±£³ÖĢå»ż²»±ä£¬¼ÓÉŁĮæĢ¼·Ū d.±£³ÖĪĀ¶ČĢå»ż²»±ä£¬Ōö“óCOÅضČ
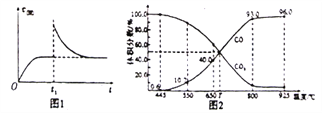
(3)ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ĻņijĢå»żæɱäµÄŗćŃ¹ĆܱÕČŻĘ÷(P×Ü)¼ÓČė1molCO2Óė×ć×īµÄĢ¼£¬·¢Éś·“Ó¦iii£¬Ę½ŗāŹ±ĢåĻµÖŠĘųĢåĢå»ż·ÖŹżÓėĪĀ¶ČµÄ¹ŲĻµČēĶ¼2ĖłŹ¾”£
¢Ł650”ꏱ£¬øĆ·“Ó¦“ļĘ½ŗāŗóĪüŹÕµÄČČĮæŹĒ__________”£(¼ĘĖ揱²»æ¼ĀĒĪĀ¶Č¶Ō”÷HµÄÓ°Ļģ)
¢ŚT”ꏱ£¬ČōĻņĘ½ŗāĢåĻµÖŠŌŁ³äČėŅ»¶ØĮæ°“v(CO2):V(CO)=5:4µÄ»ģŗĻĘųĢå£¬Ę½ŗā______(Ģī”°ÕżĻņ”±”¢”±ÄęĻņ”±»ņ”°²»”±)ŅĘ¶Æ”£
¢Ū925”ꏱ£¬ÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č±ķŹ¾µÄ»ÆŃ§Ę½ŗā³£ŹżKpĪŖ_____”£[ĘųĢå·ÖŃ¹(p·Ö)=ĘųĢå×ÜŃ¹(p×Ü)”ĮĢå»ż·ÖŹż£¬ÓĆijĪļÖŹµÄĘ½ŗā·ÖŃ¹»ÆĢęĪļÖŹµÄĮæÅضČŅ²æÉŅŌ±ķŹ¾»ÆŃ§Ę½ŗā³£Źż£¬¼Ē×÷Kp]
(4)ÓĆŌµē³ŲŌĄķæÉŅŌ³żČ„ĖįŠŌ·ĻĖ®ÖŠµÄČżĀČŅŅĻ©”¢AsO3-£¬ĘäŌĄķČēĶ¼3ĖłŹ¾(µ¼µēæĒÄŚ²æĪŖÄÉĆ×Įć¼ŪĢś)”£
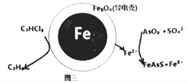
ŌŚ³żĪŪ¹ż³ĢÖŠ£¬ÄÉĆ×Įć¼ŪĢśÖŠµÄFeĪŖŌµē³ŲµÄ____¼«(Ģī”°Õż”±»ņ”°øŗ”±)£¬Š“³öC2HCl3ŌŚĘä±ķĆę±»»¹ŌĪŖŅŅĶéµÄµē¼«·“Ó¦Ź½ĪŖ____________________”£
(5)NaHSæÉÓĆÓŚĪŪĖ®“¦ĄķµÄ³Įµķ¼Į”£ŅŃÖŖ:25”ꏱ£¬·“Ó¦Hg2+(aq)+HS-(aq) ![]() HgS(s)+H+(aq)µÄĘ½ŗā³£ŹżK=1.75”Į1038£¬H2SµÄµēĄėĘ½ŗā³£ŹżKa1=1.0”Į10-7£¬Ka2=7.0”Į10-15”£
HgS(s)+H+(aq)µÄĘ½ŗā³£ŹżK=1.75”Į1038£¬H2SµÄµēĄėĘ½ŗā³£ŹżKa1=1.0”Į10-7£¬Ka2=7.0”Į10-15”£
¢ŁNaHSµÄµē×ÓŹ½ĪŖ____________________”£
¢ŚKsp(HgS)=_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĆܱÕČŻĘ÷ÖŠ³äČėCOŗĶCO2µÄ»ģŗĻĘųĢ壬ĘäĆܶȏĒĻąĶ¬Ģõ¼žĻĀŗ¤ĘųĆܶȵÄ8±¶£¬ÕāŹ±²āµĆČŻĘ÷ÄŚŃ¹ĒæĪŖP1£¬ČōæŲÖĘČŻĘ÷µÄĢå»ż²»±ä£¬¼ÓČė×ćĮæµÄ¹żŃõ»ÆÄĘ£¬²¢²»¶ĻÓƵē»š»ØµćČ¼ÖĮĶźČ«·“Ó¦£¬»Öø“µ½æŖŹ¼µÄĪĀ¶Č£¬ŌŁ“Ī²āµĆČŻĘ÷ÄŚµÄŃ¹ĒæĪŖP2£¬ŌņP1ŗĶP2¹ŲĻµŹĒ
A. P1=8P2 B. P1=4P2 C. P1=2P2 D. P1=P2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀµÄŗćĪĀŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦X(g)+3Y(g)![]() 2Z(g)£¬ČōX”¢Y”¢ZµÄĘšŹ¼ÅØ¶Č·Ö±šĪŖc1”¢c2”¢c3(¾ł²»ĪŖĮć)£¬“ļµ½Ę½ŗāŹ±£¬X”¢Y”¢ZµÄÅØ¶Č·Ö±šĪŖ0.1mol/L”¢0.3mol/L”¢0.08mol/L”£ŌņĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
2Z(g)£¬ČōX”¢Y”¢ZµÄĘšŹ¼ÅØ¶Č·Ö±šĪŖc1”¢c2”¢c3(¾ł²»ĪŖĮć)£¬“ļµ½Ę½ŗāŹ±£¬X”¢Y”¢ZµÄÅØ¶Č·Ö±šĪŖ0.1mol/L”¢0.3mol/L”¢0.08mol/L”£ŌņĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
A. c1:c2=1:2 B. Ę½ŗāŹ±£¬YŗĶZµÄÉś³ÉĖŁĀŹÖ®±ČĪŖ2£ŗ3
C. Čō·“Ó¦ÕżĻņ½ųŠŠ£¬X”¢YµÄ×Ŗ»ÆĀŹ²»ĻąµČ D. c1µÄȔֵ·¶Ī§ĪŖ0<c1<0.14mol/L
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com