
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
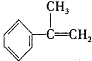 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式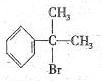 .
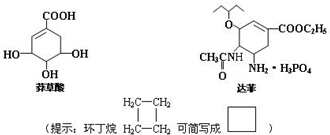
.
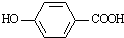 ),其反应类型为:消去反应;
),其反应类型为:消去反应;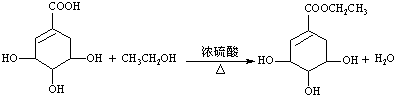 .
. 分析 (1)(2)有机物的结构决定其性质,分析表中数据可以看出,当乙烯分子中的H原子被甲基取代时,反应速率加快,且甲基个数越多,反应速率越快;当乙烯分子中的H原子被卤原子取代时,反应速率减慢,以此解答该题;
(3)a.根据结构简式判断官能团;
b.A中含-OH,-OH减少,有不饱和键生成;
c.莽草酸与乙醇反应为酯化反应.
解答 解:(1)分析表中数据可知,反应速率与C=C中烃基的个数有关,烃基越多,反应速率越大,并且当C=C上取代基为卤素原子的反应速率慢,卤素原子越多反应速率越慢,由于(CH3)2C=C(CH3)2的烃基最长,且不含卤素原子,反应最快,此烃为烯烃,最长碳链为4,在2、3号碳之间含有1个碳碳双键,在23号碳上分别含有1个甲基,正确命名为:2,3-二甲基-2-丁烯,故答案为:A;
(2)由所给信息:CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2Br(次要产物),Br加在中间碳山为主要产物,加在端点碳上为次要产物,那么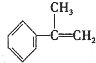 的主要加成产物为:
的主要加成产物为: ,故答案为:
,故答案为: ;
;
(3)a.莽草酸含有的官能团有羟基、羧基、碳碳双键,故答案为:羟基、羧基、碳碳双键;
b.莽草酸在浓硫酸作用下加热可以得到B,-OH减少,有不饱和键生成,则为醇的消去反应,故答案为:消去反应;
c.莽草酸与乙醇反应为酯化反应,该反应为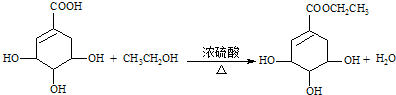 ,
,
故答案为: .
.
点评 本题综合有机化学知识和化学反应速率知识以及有机物的官能团的性质,通过分析数据总结出规律,再用此规律解决问题,这是本题最大的特点,本题综合考查了重要的烃和烃的含氧衍生物的性质、相互转化关系.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:填空题
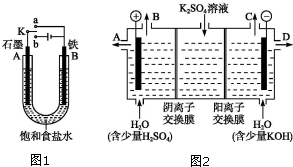 某课外活动小组用如图装置进行实验,试回答下列问题:
某课外活动小组用如图装置进行实验,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅的结构类似于金刚石 | |
| B. | 硅是良好的半导体材料 | |
| C. | 硅的性质较稳定,在自然界中存在游离态 | |
| D. | 可以用焦炭还原二氧化硅生成硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16 | B. | 17 | C. | 18 | D. | 15 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铵溶液呈酸性:NH4+═NH3+H+ | |
| B. | 氢硫酸的电离:H2S?2H++S2-? | |
| C. | 向小苏打溶液中加入醋酸溶液:HCO3-+H+?CO2+H2O | |
| D. | 在标准状况下,向10 mL 0.1 mol•L-1 FeBr2溶液中通入22.4 mL Cl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2→O2 | B. | FeCl2→FeCl3 | C. | KClO3→O2 | D. | Al2O3→AlO${\;}_{2}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ | |
| C. | 由C(石墨)=C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定 | |
| D. | 能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com