
下列说法正确的是:
A.阴离子中可能含有金属元素,阳离子一定由金属元素组成
B.由金属元素和非金属元素形成的化合物一定是离子化合物
C.只含有非金属元素的化合物只能是共价化合物
D.两个非金属原子间不可能形成离子化合物
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
(2013?徐州模拟)某温度下,反应2A(g)
|
查看答案和解析>>
科目:高中化学 来源: 题型:
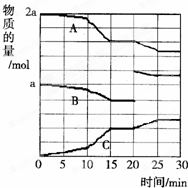 在实验室中做下列实验:把物质A、B按一定比例充入一个表面积为300cm2,容积为2L的球形容器,使压强为P,然后将整个容器用加热器加热到t℃时,发生如下反应:
在实验室中做下列实验:把物质A、B按一定比例充入一个表面积为300cm2,容积为2L的球形容器,使压强为P,然后将整个容器用加热器加热到t℃时,发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | A | ||||||
| 2 | B | C | D | E | J | K | L |
| 3 | F | G | H | I | |||
| M |
 它的空间利用率为
它的空间利用率为查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 碳是形成化合物最多的元素.
碳是形成化合物最多的元素.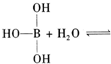
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com