
| A. | 第14列元素的最高价氧化物的化学式为RO2 | |
| B. | 第2列元素中一定没有非金属元素 | |
| C. | 在18列元素中,第3列元素种类最多 | |
| D. | 第15列元素的最高价氧化物对应水化物的化学式均为H3RO4 |
分析 A.第14列元素的最高价氧化物的化学式为RO2;
B.第2列元素为ⅡA族元素,为碱土金属元素;
C.在18列元素中,第3列为ⅢB族,有镧系和锕系;
D.第15列元素为ⅤA族元素.
解答 解:A.第14列元素是第ⅣA族元素,最高正化合价是+4价,所以最高价氧化物的化学式为RO2,故A正确;
B.第2列元素为ⅡA族元素,为碱土金属元素,全为金属元素,则没有非金属元素,故B正确;
C.在18列元素中,第3列为ⅢB族,有镧系和锕系,则元素种类最多,故C正确;
D.第15列元素为ⅤA族元素,最高价为+5价,N元素的最高价氧化物对应水化物的化学式为HNO3,故D错误;
故选D.
点评 本题考查元素周期表的结构,熟悉族和列的关系是解答本题的关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 在由水电离产生的C(OH-)=1×10-12 mol•L-1的溶液中,K+、Al3+、SO42-、Cl-一定可以大量共存 | |
| B. | 由0.1 mol/L一元碱BOH溶液的pH=10,可推知BCl溶液呈酸性 | |
| C. | 在pH=0的溶液中,K+、Fe2+、Cl-、NO3-可以大量共存 | |
| D. | 含碳酸氢钠的溶液:K+、SO42-、Cl-、H+能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素元素都有正化合价 | B. | 卤素元素的单质都只具有氧化性 | ||
| C. | 卤素元素的最低化合价都是-1价 | D. | 卤素元素氢化物都是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③①④ | B. | ③②①④ | C. | ③①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

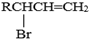
 .
. .
.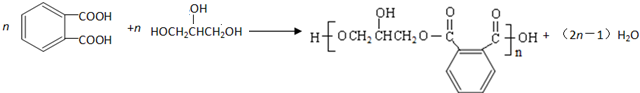 .
.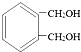 互为同分异构体的结构简式
互为同分异构体的结构简式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚氯乙烯塑料强度大,抗腐蚀性强,可以用来包装需长时间保存的食品 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 油脂、淀粉、纤维素、蛋白质都属于天然有机高分子材料 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
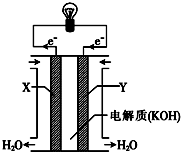 一个完整的氧化还原反应的方程式可以拆开,写成两个“半反应式”,一个是氧化反应式,另一个是还原反应式.如2Fe3++Cu═2Fe2++Cu2+的拆写结果是:
一个完整的氧化还原反应的方程式可以拆开,写成两个“半反应式”,一个是氧化反应式,另一个是还原反应式.如2Fe3++Cu═2Fe2++Cu2+的拆写结果是:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com