
下列说法正确的是
A.NaHCO3溶液中:c(H+)+c(Na+) = c(OH-)+c(CO32 -)+c(HCO3- )
B.常温下,等物质的量浓度的 (NH4)2CO3 和Na2CO3溶液,前者的c(HCO3- )小
C.常温下,pH =3的CH3COOH与pH =11的NaOH溶液等体积混合后的溶液中:c(OH-)<c(H+)
D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后溶液呈酸性:c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C
【解析】
试题分析:A中NaHCO3溶液呈电中性,根据电荷守恒,c(H+)+c(Na+) = c(OH-) +2c(CO32 -)+c(HCO3- ),错误;B中常温下,等物质的量浓度的 (NH4)2CO3 和Na2CO3溶液,NH4+ 水解显酸性,促进了CO32 -的水解,而Na+对CO32 -的水解无影响,所以前者的c(HCO3- )大,错误;C中醋酸是弱酸,常温下,pH =3的CH3COOH溶液中电离出来的H+浓度为10-3mol/L,而醋酸的浓度大于10-3mol/L,NaOH是强碱,pH =11的NaOH溶液中,OH-的浓度为10-3mol/L,两者等体积混合后,溶液是醋酸与醋酸钠的混合溶液,显酸性:c(OH-)<c(H+),正确;D中物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后溶液呈酸性,说明水解能力小于醋酸的电离能力,各微粒关系应为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-),错误;选C。
考点:考查盐溶液中离子浓度的大小关系,pH的计算与溶液的酸碱性等知识。


科目:高中化学 来源:2014-2015浙江省高一上学期期末联考化学试卷(解析版) 题型:填空题
(6分)比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如2Na2O2+2CO2 == 2Na2CO3+O2,Na2O2+CO= Na2CO3。
(1)通过比较可知,当非金属元素处于____________价时,其氧化物与Na2O2反应有O2生成。
(2)试分别写出Na2O2与SO2、SO3反应的化学方程式:_____________;_____________。
(3)氰(CN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二上学期期末联考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使甲基橙呈红色的溶液中:K+、AlO2-、NO3-、CO32-
B.c(ClO-)=1.0 mol·L-1溶液:Na+、SO32-、S2-、Cl-
C.水电离出来的c(H+)=1×10-12的溶液:K+、NH4+、SO42-、Fe3+
D.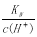 =0.1 mol·L-1的溶液:Na+、AlO2-、CO32-、NO3-
=0.1 mol·L-1的溶液:Na+、AlO2-、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015云南省高二上学期期末考试化学试卷(解析版) 题型:选择题
室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是
A、0.1 mol/L盐酸和0.1 mol/L氢氧化钠溶液
B、0.1 mol/L硫酸和0.1 mol/L氢氧化钡溶液
C、pH=4的醋酸溶液和pH=10的氢氧化钠溶液
D、pH=4的盐酸和pH=10的氨水
查看答案和解析>>
科目:高中化学 来源:2014-2015云南省高二上学期期末考试化学试卷(解析版) 题型:选择题
用惰性电极电解饱和食盐水,当电源供给0.2 mol电子时,停止通电。若此溶液体积为2 L,则所得电解液的pH是
A、1 B、8 C、13 D、14
查看答案和解析>>
科目:高中化学 来源:2014-2015云南省高二上学期期末考试化学试卷(解析版) 题型:选择题
已知:C (s)+ O2(g)=CO(g) H= -110. 50KJ/mol
C (s)+O2(g)=CO2(g) H= -393.51KJ/mol
则反应C (s)+CO2(g)= 2 CO(g)的H为
A、-283.01KJ/mol B、+172.51 KJ/mol
C、+283.01KJ/mol D、-504.01 KJ/mol
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省攀枝花市高二上学期期末考试化学试卷(解析版) 题型:填空题
(8分)孔雀石的主要成分为Cu2(OH)2CO3,还含少量铁的氧化物和硅的氧化物。以下是实验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:
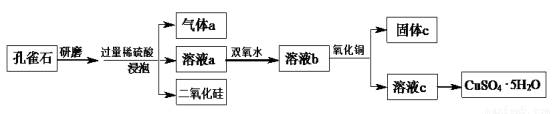
请回答下列问题:
(1)研磨孔雀石的目的是 。
(2)加入双氧水的目的是将溶液中的Fe2+转化为Fe3+,相应的离子方程式为 。
(3)固体c中主要成分的化学式为 。加入氧化铜的作用是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省攀枝花市高二上学期期末考试化学试卷(解析版) 题型:选择题
Cu与Zn用导线连接后浸入稀硫酸组成原电池装置。当导线中有0.5mol电子通过时,理论上两极的变化正确的是
A.锌为负极,锌片溶解32.5g
B.铜为正极,铜片上产生0.25mol的H2
C.电子由铜极经导线流向锌极
D.溶液中SO42-定向移向铜极
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省吉安市高一上学期期末考试化学试卷(解析版) 题型:选择题
HO2(超氧酸)是一种弱酸,具有极高的活性。一定条件下,铜与盐酸、氧气发生如下反应可生成 ,下列说法正确的是
,下列说法正确的是
A.上述反应中,O2发生了氧化反应
B.HO2在碱溶液中能稳定存在
C.上述反应中HO2是还原产物
D.上述反应的离子方程式为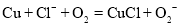
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com