
【题目】PCl3是制造有机磷农药和磺胺嘧啶类医药的原料,其制备方法是将熔融黄磷(P4)与干燥氯气进行氯化反应。
(1) PCl3遇水会强烈水解,写出PCl3与水反应的化学方程式:________。
(2) 制得的PCl3粗产品中常含有POCl3、PCl5等杂质。通过实验测定粗产品中PCl3的质量分数,实验步骤如下(不考虑杂质的反应):
a. 迅速移取20.00 g PCl3粗产品,加水完全水解后,再配成500.00 mL溶液;
b. 量取所配溶液25.00 mL于碘量瓶中,加入0.500 0 mol·L-1碘溶液20.00 mL和1.000 mol·L-1(NH4)3BO3溶液30.00 mL,振荡;
c. 加入2~3滴淀粉溶液,用1.000 0 mol·L-1 Na2S2O3标准溶液滴定过量的碘,滴至终点时消耗Na2S2O3标准溶液12.00 mL。
已知测定过程中的部分反应为H3PO3+H2O+I2![]() H3PO4+2HI,3HI+(NH4)3BO3===3NH4I+H3BO3,I2+Na2S2O3―→Na2S4O6+NaI(未配平)。
H3PO4+2HI,3HI+(NH4)3BO3===3NH4I+H3BO3,I2+Na2S2O3―→Na2S4O6+NaI(未配平)。
①步骤b中加入(NH4)3BO3溶液的目的是________。
②判断步骤c中滴定终点的方法为________。
③根据上述数据,计算制得粗产品中PCl3的质量分数(写出计算过程)。_________
【答案】PCl3+3H2O=H3PO3+3HCl 减小HI浓度,平衡右移,使H3PO3被I2充分氧化成H3PO4 当滴入最后一滴1.000 0 mol·L-1 Na2S2O3标准溶液时,溶液由蓝色突变为无色,且半分钟内不变色 n(I2)=0.500 0 mol·L-1×20.00 mL×10-3 L·mL-1=0.010 00 mol,n(Na2S2O3)=1.000 mol·L-1×12.00 mL×10-3 L·mL-1=0.012 00 mol,与Na2S2O3反应的n(I2)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() ×0.012 00 mol=0.006 00 mol,n(H3PO3)=0.010 00 mol-0.006 00 mol=0.004 00 mol,n(PCl3)=n(H3PO3)=0.004 00 mol,w%=
×0.012 00 mol=0.006 00 mol,n(H3PO3)=0.010 00 mol-0.006 00 mol=0.004 00 mol,n(PCl3)=n(H3PO3)=0.004 00 mol,w%=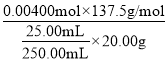 ×100%=55.00%
×100%=55.00%
【解析】
(1) PCl3遇水会强烈水解生成磷酸和盐酸;
(2) ①已知反应H3PO3+H2O+I2H3PO4+2HI,磷酸中的磷来自于三氯化磷的水解,结合实验目的分析;
②结合碘遇淀粉变蓝分析;
③该实验原理为:利用PCl3遇水生成H3PO3和HCl,加入碘溶液,发生反应H3PO3+H2O+I2H3PO4+2HI,然后加入(NH4)3BO3溶液,与HI和H3PO4反应生成H3BO3,最后利用Na2S2O3溶液滴定为反应的I2,根据消耗的I2,计算PCl3的质量,进而确定样品中PCl3的质量分数。
(1) PCl3遇水会强烈水解生成磷酸和盐酸,化学反应方程式为:PCl3+3H2O=H3PO3+3HCl;
(2)①本实验要准确测定样品中PCl3的纯度,反应H3PO3+H2O+I2H3PO4+2HI,磷酸中的磷来自于三氯化磷的水解,加入(NH4)3BO3,发生反应3HI+(NH4)3BO3=3NH4I+H3BO3,减小HI浓度,平衡右移,使H3PO3被I2充分氧化成H3PO4,生成磷酸越多,PCl3的纯度越高;
②碘遇淀粉变蓝,Na2S2O3标准溶液与碘反应,当将过量的碘消耗完,蓝色消失,则判定终点的方法为:当滴入最后一滴1.000 0 mol·L-1 Na2S2O3标准溶液时,溶液由蓝色突变为无色,且半分钟内不变色,即为到达终点;
③20.00 mL 0.5000 mol·L-1碘溶液中,碘单质的总物质的量=0.5000 mol·L-1×20.00 mL×10-3 L·mL-1=0.01000 mol,滴定时消耗的标准液的n(Na2S2O3)=1.000 mol·L-1×12.00 mL×10-3 L·mL-1=0.012 00 mol;根据滴定反应:I2+2Na2S2O3=Na2S4O6+2NaI,过量的碘单质的物质的量=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() ×0.01200 mol=0.00600 mol;根据反应H3PO3+H2O+I2H3PO4+2HI,25.00 mL样品水解液中,与碘应的n(H3PO3)=n(I2)=0.01000 mol-0.00600 mol=0.00400 mol;结合反应PCl3+3H2O=H3PO3+3HCl,25.00 mL样品水解液中,完全发生水解的n(PCl3)=n(H3PO3)=0.00400 mol,500mL样品水解液中,完全发生水解的n(PCl3)=0.00400 mol×
×0.01200 mol=0.00600 mol;根据反应H3PO3+H2O+I2H3PO4+2HI,25.00 mL样品水解液中,与碘应的n(H3PO3)=n(I2)=0.01000 mol-0.00600 mol=0.00400 mol;结合反应PCl3+3H2O=H3PO3+3HCl,25.00 mL样品水解液中,完全发生水解的n(PCl3)=n(H3PO3)=0.00400 mol,500mL样品水解液中,完全发生水解的n(PCl3)=0.00400 mol×![]() ,则原样品中w%=
,则原样品中w%=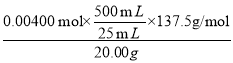 ×100%=55.00%。
×100%=55.00%。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】某温度下在密闭容器中发生如下可逆反应:2M(g)+N(g)![]() 2E(g),若开始时只充入2mol E(g),达平衡时,E的转化率为40%;若开始时充入2mol M和1mol N的混合气体,达平衡时混合气体的压强比起始时减少了( )
2E(g),若开始时只充入2mol E(g),达平衡时,E的转化率为40%;若开始时充入2mol M和1mol N的混合气体,达平衡时混合气体的压强比起始时减少了( )
A.20%B.40%C.60%D.80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中的氮氧化物![]() 、
、![]() 、
、![]() 等的含量高低是衡量空气质量优劣的重要指标,对其研究和综合治理具有重要意义。
等的含量高低是衡量空气质量优劣的重要指标,对其研究和综合治理具有重要意义。
![]() 汽车发动机工作时会引发反应:
汽车发动机工作时会引发反应:![]() ,
,![]() ,其能量变化示意图如下:
,其能量变化示意图如下:
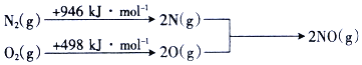
则NO中氮氧键的键能为______![]() 。
。
![]() 以碱液为电解质可实现如下转化:
以碱液为电解质可实现如下转化:![]()
![]()
![]() ,
,![]() 该反应在一定条件下能自发进行的原因是______,阴极反应式为______。
该反应在一定条件下能自发进行的原因是______,阴极反应式为______。
![]() 将
将![]() 和
和![]() 溶于水可得到相应的酸
溶于水可得到相应的酸![]() 时,两种酸的电离平衡常数如表:
时,两种酸的电离平衡常数如表:
|
| |
|
|
|
|
|
|
①![]() 的水解平衡常数为______。
的水解平衡常数为______。
②![]() 溶液和
溶液和![]() 溶液反应的离子方程式为______。
溶液反应的离子方程式为______。
![]() 汽车尾气处理催化装置中涉及的反应之一为:
汽车尾气处理催化装置中涉及的反应之一为:![]() ,
,![]() 研究表明,在使用等质量的催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某科研小组设计了以下三组实验:
研究表明,在使用等质量的催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某科研小组设计了以下三组实验:
实验 编号 |
| NO初始浓度 | CO初始浓度 | 催化剂比表面积 |
Ⅰ | 400 |
|
| 82 |
Ⅱ | 400 |
|
| 124 |
Ⅲ | 450 |
|
| 124 |
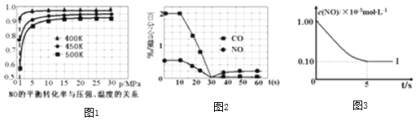
根据下列坐标图,计算前5s内用![]() 表示的反应速率为______;并在坐标图中画出上表实验Ⅱ、Ⅲ条件下,混合气体中NO浓度随时间变化的趋势
表示的反应速率为______;并在坐标图中画出上表实验Ⅱ、Ⅲ条件下,混合气体中NO浓度随时间变化的趋势![]() 标明各条曲线的实验编号
标明各条曲线的实验编号![]() 。______
。______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.10 mol·L-1标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
实验 序号 | 待测液 体积/mL | 所消耗NaOH标准液的体积/mL | |
滴定前读数/mL | 滴定后读数/mL | ||
1 | 20.00 | 0.50 | 20.54 |
2 | 20.00 | 6.00 | 26.00 |
3 | 20.00 | 1.40 | 21.36 |

(1)滴定时选用酚酞试液作指示剂,如何判断滴定达到终点____________。
(2)滴定过程中,眼睛应注视_____________________;
(3)盐酸的物质的量浓度为___________。
(4)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是__________(填“偏高”“偏低”或“无影响”)。
(5)某同学用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,高锰酸钾溶液应盛放在________(填“甲”或“乙”)中,该反应的离子方程式为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 NaHCO3溶液:Na+、Ba2+、NO3-、OH-
B.0.1 mol·L-1NaAlO2溶液:K+、OH-、Cl-、NO3-
C.常温下,![]() =1.0×1012的溶液:Fe2+、Mg2+、NO3-、Cl-
=1.0×1012的溶液:Fe2+、Mg2+、NO3-、Cl-
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO32-、S2-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是![]() 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:

回答下列问题:
(1)A的结构简式为_______。
(2)D分子中最多有_____个碳原子共平面,与D化学式相同且符合下列条件的同分异构体有__种。(①与D具有相同的官能团,②苯环上的三元取代物)
(3)①的反应类型是________。
(4)⑤的化学方程式为________。
(5)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线:______________。
的合成路线:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积为2L的两个恒容容器中发生:![]() 均为气态物质
均为气态物质![]() 有下表所示实验数据:
有下表所示实验数据:
容器编号 | 起始时各物质的物质的量 | 达到平衡时体系能量的变化 | ||
|
|
| ||
① | 1 | 3 | 0 |
|
② | 0 | 0 | 2 |
|
③ |
|
|
|
|
下列有关说法正确的是
A.![]()
B.②中![]() 的转化率大于③中
的转化率大于③中![]() 的转化率
的转化率
C.容器①与③分别达到平衡时,平衡常数相同,且![]()
D.将容器①的反应条件换为恒温恒压中进行![]() 投料量不变
投料量不变![]() ,达到平衡时,气体平均摩尔质量较恒温恒容时减小了
,达到平衡时,气体平均摩尔质量较恒温恒容时减小了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国采用长征三号甲运载火箭成功发射了 “嫦娥一号” 卫星。肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气。已知:N2(g)+2O2(g)=N2O4(g) △H =+8.7kJ/mol,N2H4(g)+O2(g)=N2(g)+2H2O(g) △H= -534kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是 ( )
A.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(l) △H=–1059.3 kJ/mo
B.N2H4(g) + ![]() N2O4(g) =
N2O4(g) =![]() N2(g) + 2H2O(g) △H=–542.7 kJ/mol
N2(g) + 2H2O(g) △H=–542.7 kJ/mol
C.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–542.7 kJ/mol
D.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–1076.7 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对含微量![]() 的某样品进行
的某样品进行![]() 化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用
化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用![]() 标准溶液滴定以求得
标准溶液滴定以求得![]() 的浓度。下列分析正确的是
的浓度。下列分析正确的是
已知:![]() 过量
过量![]()
方法一![]() 样品
样品![]()
![]()
![]() -
-![]()
![]()
![]()
![]()
![]()
方法二![]() 样品
样品![]()
![]() I2
I2![]()
![]()
A.方法二对样品所做处理操作简便,用作微量的测定更准确
B.当待测液由无色变为蓝色时即达到滴定终点
C.方法一与方法二测量出的样品浓度比为6:l
D.假设各步骤操作均得当,方法一所消耗![]() 标准溶液的体积是方法二的6倍
标准溶液的体积是方法二的6倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com