
将两个铂电极插入500 mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064 g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化),此时溶液中氢离子浓度约为( )
A.4×10-3 mol·L-1 B.2×10-3 mol·L-1
C.1×10-3 mol·L-1 D.1×10-7 mol·L-1
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
分析下列各项结构的规律,按此规律排布第10项的分子式应为( )
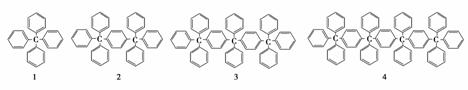
A.C198H146 B.C196H155
C.C196H146 D.C198H155
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(用推断出的元素符号回答问题)
(1)Z位于元素周期表第 周期第 族,Y的氢化物电子式是 。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。在H—Y、H—Z两种共价键中,键的极性较强的是 ,键长较长的是 ,对应氢化物较稳定的是 。
(3)写出X的单质与Y的最高价氧化物对应水化物的浓溶液反应的方程式 。
(4)写出W元素的原子核外价电子排布式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象描述正确的是( )
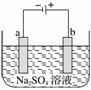
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。
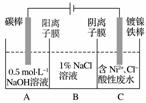
下列说法不正确的是( )
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A.碳棒上发生的电极反应:4OH--4e-===O2↑+2H2O
B.电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)[2014·四川理综,11(4)]MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“神舟七号”成功登天标志着我国的航天事业进入了新的篇章。
(1)某空间站局部能量转化系统如下图所示,其中燃料电池采用KOH溶液为电解液,燃料电池放电时的负极反应式为______________________________________。如果某段时间内氢氧储罐中共收集到33.6 L(已折算成标况)气体,则该段时间内水电解系统中转移电子的物质的量为__________mol。
向日面时 背日面时
 —→
—→ —→
—→ —→
—→
(2)在载人航天器的生态系统中,不仅要求分离出CO2,还要求提供充足的O2。某种电化学装置可实现转化2CO2===2CO+O2,CO可用作燃料。已知该反应的阳极反应式为4OH--4e-===O2↑+2H2O,则阴极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.FeO固体放入稀硝酸中:
FeO+2H+===Fe2++H2O
B.过量的铁粉与稀硝酸反应:
Fe+4H++NO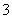 ===Fe3++NO↑+2H2O
===Fe3++NO↑+2H2O
C.向氢氧化亚铁中加入足量的稀硝酸:
Fe(OH)2+2H+===Fe2++2H2O
D.向Fe(OH)3中加入氢碘酸:
2Fe(OH)3+6H++2I-===2Fe2++I2+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com