
| A. | 凡需加热的反应一定是吸热反应 | |
| B. | 相同条件下,2molH2(g)与lmolO2(g)完全化合生成2molH2O(g),放出aKJ热量,2molH2 (g)与lmolO2(g)完全化合生成2molH2O(l),放出bkJ 热量,则a>b | |
| C. | 若CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 | |
| D. | 相同条件下,1molH2O(l)与1molCaO完全化合,放出a kJ热量,2molH2O(l)与2molCaO完全化合,也放出a kJ热量 |
分析 A.化学反应的能量变化是由反应物总能量和生成物总能量的相对大小决定,吸热反应说明生成物的总能量大于反应物总能量,加热的反应不一定是吸热反应;
B.2molH2(g)和1molO2(g)完全化合成2molH2O(g)所放出的热量比在相同条件下2molH2(g)和1molO2(g)完全化合成2molH2O(l)所放出的热量少;
C.一个化学反应其正、逆反应的能最变化,在数值上相等,吸收与放出相反;
D.反应热与参加反应的物质的物质的量成正比.
解答 解:A.加热的反应不一定是吸热反应,比如燃烧,燃烧反应多数需要加热,通过加热达到着火点,但为放热反应,故A错误;
B.H2O(g)═H2O(l)是放热过程,2molH2(g)和1molO2(g)完全化合成2molH2O(g)所放出的热量比在相同条件下2molH2(g)和1molO2(g)完全化合成2molH2O(l)所放出的热量少,则a<b,故B错误;
C.CO2与CaO化合,与CaCO3分解,属于同一个化学反应其正、逆反应,正、逆反应的能最变化,在数值上相等,符号相反,若CO2与CaO化合是放热反应,则CaCO3分解是吸热反应,故C正确;
D.相同条件下,1molH2O(l)与1molCaO完全化合,放出a kJ热量,2molH2O(l)与2molCaO完全化合,放出2a kJ热量,故D错误;
故选C.
点评 本题考查了反应的类型与能量变化的关系,题目难度不大,注意反应热与参加反应的物质的物质的量成正比,一个化学反应其正、逆反应的能最变化,在数值上相等,吸收与放出相反.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸 | |
| B. | 分离苯和硝基苯的混合物,可用蒸馏法 | |
| C. | 除去苯中的杂质苯酚可加入浓溴水后过滤 | |
| D. | 从粗苯甲酸中提纯苯甲酸,可用重结晶法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
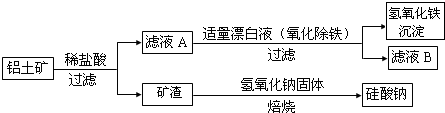
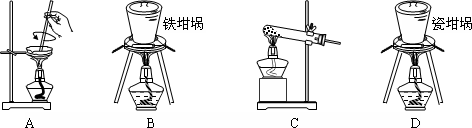
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +2 | B. | +4 | C. | 0 | D. | +6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示.
T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{r(Na)}{r(N{a}^{+})}$ | B. | $\frac{r({F}^{-})}{r({O}^{2-})}$ | C. | $\frac{r(Na)}{r(Mg)}$ | D. | $\frac{r(Ca)}{r(Mg)}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠和葡萄糖分别溶解在水中 | B. | 干冰和氯化铵分别受热变为气体 | ||
| C. | 食盐和冰分别受热熔化 | D. | 液溴和酒精分别挥发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 操作 |
| A | 配制100mL1.0mol•L-1CuSO4 溶液 | 将25.0gCuSO4•5H2O溶于蒸馏水配成100mL溶液 |
| B | 除去KNO3固体中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C | 检验溶液是否含有SO42- | 取少量待测液于试管中,加入硝酸酸化的Ba(NO3)2溶液 |
| D | 检验溶液中是否含有NH4+ | 取少量溶液于试管中,加入NaOH后,加热,在试管口放置一片湿润的红色石蕊试纸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com