
(1)被还原的HNO3的物质的量。
(2)合金中银的质量分数。
科目:高中化学 来源: 题型:阅读理解
| △ |
| △ |
| x |
| y |
| 2(a-b) |
| 7b |
| 2(a-b) |
| 7b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 9b |
| 17a |
| 9b |
| 17a |
查看答案和解析>>
科目:高中化学 来源: 题型:
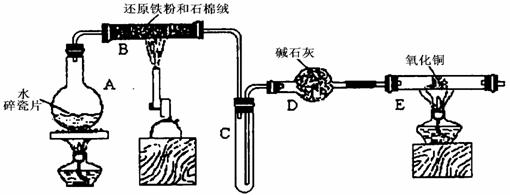 某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器)。
某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器)。
(1) 给硬质玻璃管B加热的仪器名称是_________
(2)B中发生反应的化学方程式是__________________________________________________。
(3)为了安全,加热E以前必须进行的操作是________________________________________。
(4)已知有反应:Cu20+2H+![]() Cu+Cu2++H20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu20,可用的试剂是________(填序号)
Cu+Cu2++H20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu20,可用的试剂是________(填序号)
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的相对原子质量。若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg。
①水中元素的物质的量之比可表示为(不用化简)n(H):n(0)= ________:_______;若反应后E中除Cu外还含有另种还原产物Cu20,则该比值将___________ (选填“偏大”“偏小”或“无影响”)。
②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的相对原子质量可表示为______________________________。
(6)某学生为了检验反应后固体的成分,反应前在E管中加入了氧化铜16g,反应后称量固体的质量变为13.6g,则13.6g的成分为:____________(若为混合物,需计算出各自的质量)
查看答案和解析>>
科目:高中化学 来源: 题型:
某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器)。
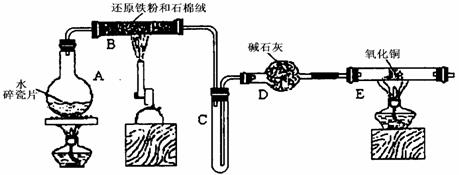
(1) 给硬质玻璃管B加热的仪器名称是_________
(2)B中发生反应的化学方程式是___________________________________________。
(3)为了安全,加热E以前必须进行的操作是_________________________________。
(4)已知有反应:Cu2O+2H+![]() Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的摩尔质量。若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg。
①水中元素的物质的量之比可表示为(不用化简)n(H):n(O)= _______︰_______;若反应后E中除Cu外还含有另种还原产物Cu2O,则该比值将___________ (选填“偏大”“偏小”或“无影响”)。
②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的摩尔质量可表示为______________________________。
(6)某学生为了检验反应后固体的成分,反应前在E管中加入了氧化铜16g,反应后称量固体的质量变为13.6g,则13.6g的成分为:____________(若为混合物,需计算出各自的质量)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com