
【题目】下列反应属于氧化还原反应,且能量变化如图所示的是( ) 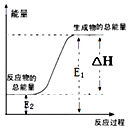
A.锌粒和稀硫酸反应
B.灼热的木炭与CO2反应
C.甲烷在空气中燃烧的反应
D.Ba(OH)28H2O晶体与NH4Cl晶体的反应
科目:高中化学 来源: 题型:
【题目】用价层电子对互斥理论预测H2S和CH2O的立体结构,两个结论都正确的是( )
A. 直线形;三角锥形 B. V形;三角锥形
C. 直线形;平面三角形 D. V形;平面三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向浓度均为01mol·L-1、体积均为100mL的两种一元酸HX、HY溶液中,分别加入NaOH的稀溶液,lg![]() 随加入NaOH的物质的量的变化如图所示。下列说法正确的是( )
随加入NaOH的物质的量的变化如图所示。下列说法正确的是( )
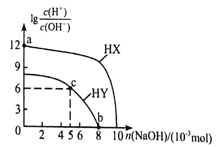
A. a点溶液的ph=2
B. 水的电离程度:a<b<c
C. b点溶液中:c(Yˉ)+c(HY)=c(Na+)
D. c点溶液中:c(Yˉ)>C(Na+)>c(HY)>c(H+)>c(OHˉ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,若关闭活塞A,则品红溶液无变化,石蕊试液变红,石灰水变浑浊;若打开活塞A,则品红溶液褪色,石蕊试液变红,石灰水变浑浊。据此判断气体和广口瓶中盛放的物质是
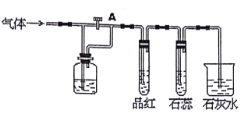
A. C12和NaHSO3溶液 B. HCl和浓H2SO4
C. C12和氯水 D. SO2和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合氯化铝([Al2( OH)nCl6-n]m}是一种新型高效净水剂,与一般絮凝剂相比,它的吸附能力强、絮凝率高,可由AlCl3经水解法制得。回答下列问题:
(1)工业上可用Cl2、Al2O3和焦炭在高温下反应制取AlCl3![]()
已知:4Al(s)+3O2(g)=2Al2O3(s) △H1
2C(s)+O2(g)=2CO(g) △H2
2Al(s)+3Cl2(g)=2A1Cl3(g) △H3
①Al2O3(s)+3C(s)+3Cl2(g) ![]() 2AlCl3(g)+3CO(g) △H=____________________。
2AlCl3(g)+3CO(g) △H=____________________。
②反应3A12O3(s)+6Cl2(g) ![]() 4AlCl3(g)+3O2(g)在高温下较难发生,但加入焦炭后可提高氯气的转化率,原因是_________________________________。
4AlCl3(g)+3O2(g)在高温下较难发生,但加入焦炭后可提高氯气的转化率,原因是_________________________________。
(2)AlCl3在水溶液中分三步水解
Al3++H2O![]() Al(OH)2++H+ K1
Al(OH)2++H+ K1
Al(OH)2++H2O![]() Al(OH)2++H+ K2
Al(OH)2++H+ K2
Al(OH)2++ H2O![]() Al(OH)3+H+ K3
Al(OH)3+H+ K3
①K1、K2、K3由小到大的顺序是_______________________。
②控制溶液的pH在一定范围内,上述水解产物才能聚合生成聚合氯化铝。pH偏小时,Al3+的水解程度弱;pH偏大时的影响是___________________________。
(3)已知有如下可逆反应: ![]()
![]()
298K时,将1mL 1 mol·L-1 AlCl3溶液与1mL2 a mol ·L-1H2QSI溶液混合发生上述反应,溶液中c[Al(HQSI)2+]与时间(t)的关系如图所示。
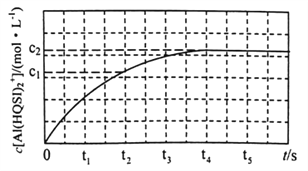
①下列可判断该反应达到平衡状态的是______________(填标号)。![]()
A.溶液的pH不再变化 B. v(Al3+)=v [Al(HQSI)2+]
C.溶液颜色不再变化 D.c(A13+)/c(H2QSI)不再变化
②0~t2时间内,该反应的平均反应速率v(H2QSI)= _________________。
③298K时,该反应的平衡常数K=_________________。
(4)该方法制得的聚合氯化铝的优点是不含其它金属离子,但盐基度低(盐基度:衡量絮凝剂絮凝效果的重要指标,定义式为:盐基度=n(OH)/3n(Al),n为物质的量)。常温下实验测量样品的盐基度,取m g样品,该样品中Al的质量分数为w;加入煮沸后冷却的蒸馏水溶解,配成1L溶液,测得该溶液pH=9.0。则其盐基度为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子结构及其性质的解释中,不正确的是( )
A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B.乳酸[CH3CH(OH)COOH]属于手性分子,因分子中存在手性碳原子
C.配合物中一定含有过渡金属原子或离子,因为过渡金属原子或离子存在空轨道
D.酸性H3PO4>HClO,是因为H3PO4分子非羟基氧原子数目比HClO多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中存在大量元素,在工农业生产中有广泛应用。回答下列问题:
(1)人工合成的蓝宝石晶体(Al2O3)是目前半导体工业中应用最广泛的材料。
①基态Al原子中有______种运动状态不同的电子,核外电子占据最高能级的符号是_____,占据该能级电子的电子云轮廓图形状为_______。
②比较第一电高能:Mg______Al(填“>”、”<”或“=”)。在现代化学中,常利用_________上的特征谱线来鉴定元素,称为光谱分析。
(2)羰基硫(COS)存在于许多种植物中,杀虫效果显著。
①1molCOS分子中含有σ键的数目为_____,其中心原子的杂化方式为_____。
②CS2、CO2、COS的分解温度由低到高的顺序为_____。
(3)NaCl 和MgO都属于离子化合物.NaC1的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是_______________。
(4)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
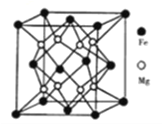
则:①距离一个Fe原子最近的Mg原子个数是______,与此晶胞结构相似的常见的离子晶体是______(填名称)。
②若该晶体储氢时,H2 分子在晶胞的体心和棱心位置,晶胞的参数为dnm,則距离最近的两个H2分子之间的距离为______cm;含铁56g的该储氢合金可储存标准状况下H2 的体积为____L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com