
| A. | 氧化还原反应的判断依据是看反应前后元素化合价是否发生变化 | |
| B. | 根据是否只含一种元素将物质分为纯净物和混合物 | |
| C. | 根据水溶液是否能导电将化合物分为电解质和非电解质 | |
| D. | 根据是否有丁达尔现象将分散系分为溶液和胶体 |
分析 A.氧化还原反应的特征是元素化合价变化;
B.根据构成物质的种类多少,把物质分为纯净物和混合物;
C.熔融状态导电性也是化合物分为电解质和非电解质的依据;
D.分散系的本质区别是分散质微粒的直径大小.
解答 解:A.氧化还原反应的特征是元素化合价变化,也是判断的依据,故A正确;
B.根据构成物质的分子多少,把物质分为纯净物和混合物,不是元素种类,故B错误;
C.区别电解质和非电解质的方法在熔融状态下的导电性,也可以区分化合物,故C错误;
D.分散系的本质区别是分散质微粒的直径大小;1nm-100nm为胶体;小于1nm为溶液,大于100nm为浊液,不是丁达尔现象,故D错误.
故选A.
点评 本题考查了氧化还原反应的特征类型应用,分散系的本质特征,电解质非电解质的本质区别,混合物的组成特征,基础题,需要熟练掌握.


科目:高中化学 来源: 题型:选择题
| A. | 要使AlCl3溶液中Al3+全部沉淀出来可使用氨水 | |
| B. | 某气体能使品红溶液褪色,该气体一定为SO2 | |
| C. | 用饱和NaHCO3溶液除去混在Cl2中的HCl气体 | |
| D. | 用Cl2除去Fe2(SO4)3溶液中的少量FeSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的熔、沸点逐渐降低 | B. | 单质的氧化性逐渐减弱 | ||
| C. | 阴离子的还原性逐渐减弱 | D. | 气态氢化物稳定性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓度均为0.01 mol•L-1的醋酸和硫酸溶液中分别加入足量锌片,生成H2的起始速率相等 | |
| B. | 0.1 mol•L-1的NaHCO3溶液中:[Na+]=[HCO3-]+[CO32-]+[H2CO3] | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:[Cl-]=[NH4+]>[OH-]=[H+] | |
| D. | 将0.1 mol的CH3COOH和0.1 mol的CH3COONa溶于水中,配成1L混合溶液.测得溶液的pH<7,则混合液中[CH3COO-]<[Na+] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③④ | C. | ①②⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
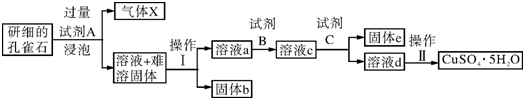
| 物质 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.8 |
| 完全沉淀时的pH | 3.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol SiO2晶体中,含有2NA个Si-O共价键 | |
| B. | 常温下,4.4 g CO2和N2O混合物中所含有的原子数为0.3NA | |
| C. | 0.2 mol Cl2溶解于等体积的水中,转移电子数为0.2NA | |
| D. | 标准状况下,11.2L 四氯化碳所含分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com