
【化学选修2-化学与技术】(15分)以硼镁矿(2Mg·B2O3·H2O·SiO2 )及少量Fe3O4、CaCO3 、Al2O3 )为原料生产硼酸的工艺流程如下:
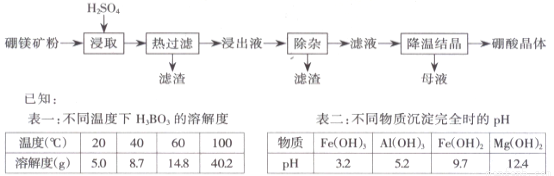
(1)由于矿粉中含CaCO3 ,“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施为_____。
(2)“浸出液”显酸性,含有H3BO3、Mg2+和SO42 -,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质。“除杂”时,向浸出液中依次加入适量目H2O2和MgO,可以除去的杂质离子为_________,H2O2 的作用为_________(用离子方程式表示)。
(3)“浸取”后,采用“热过滤”的目的为_______。
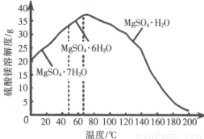
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图所示,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收 MgSO4.H2O,应采取的措施是将“母液”蒸发浓缩,____。
(5)已知25 ℃时,硼酸( H3BO3)溶液中存在如下平衡:
H3BO3(aq)+H2O(l) [B(OH)4]-(aq)+H+(aq) K=5.7×10-10;
[B(OH)4]-(aq)+H+(aq) K=5.7×10-10;
25 ℃时,0.7 mol·L-1硼酸溶液中c(H+)≈ mol·L-1.
(6)已知25 ℃时:
化学式 | H2CO3 | CH3COOH |
电离常数 | K1=4.4×10-7 K2=4.7×10-11 | K=1.75×10-5 |
下列说法正确的是_____________(填选项字母)。
A.碳酸钠溶液滴入硼酸溶液中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸溶液中能观察到有气泡产生
C.等浓度碳酸溶液和硼酸溶液的pH:前者>后者
D.等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者
科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:选择题
某学习小组的同学在学习了化学反应速率与化学平衡知识后,对反应:aA(g)+bB(g) cC(g)+dD(g)
cC(g)+dD(g) 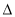 H,反应特点与对应的图象展开了讨论,其中不正确的是
H,反应特点与对应的图象展开了讨论,其中不正确的是
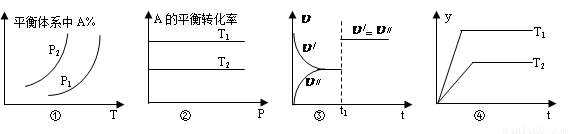
A.图①中,若P1>P2,则该反应在较低温度下有利于自发进行
B.图②中,若T2>T1,则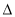 H<0且a+b=c+d
H<0且a+b=c+d
C.图③中(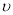 /表示正反应速率,
/表示正反应速率,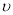 //表示逆反应速率),t1时刻改变的条件一定是使用了催化剂
//表示逆反应速率),t1时刻改变的条件一定是使用了催化剂
D.图④中,若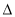 H<0,则纵坐标不可能表示的是反应物的转化率
H<0,则纵坐标不可能表示的是反应物的转化率
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三综合能力测试(五)理综化学试卷(解析版) 题型:选择题
化学与人类生活、生产和社会可持续发展密切相关,下列说法正确的是
A.为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
C.铝及其合金是电气、工业、家庭广泛使用的材料,通常用电解氯化铝的方法制取铝
D.DNOP(邻苯二甲酸二辛酯)是一种由邻苯二甲酸和正辛醇经酯化反应而得的一种酯类有机化合物,常用作增塑剂、溶剂以及气相色谱固定液,对人体无害,可用作食品添加剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期三调考试化学试卷(解析版) 题型:简答题
(14分)I.Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为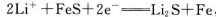 ,则该电池的总反应式为_____________________。
,则该电池的总反应式为_____________________。
Ⅱ.锂一黄铁矿高容量电池,由于其污染小、成本低、电容量大、黄铁矿储备丰富而有望取代目前市场的碱性电池。制取高纯度黄铁矿的工艺流程如下:
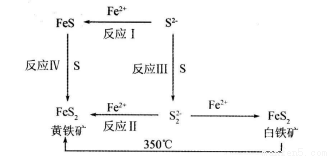
(1)已知: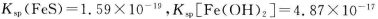 ,为得到较纯的FeS沉淀,最好在FeCl2 溶液中加入的试剂为_________(填序号)
,为得到较纯的FeS沉淀,最好在FeCl2 溶液中加入的试剂为_________(填序号)
A.(NH4)2S B.CuS C.H2S D.Na2S
(2)关于白铁矿与黄铁矿下列判断错误的是_____________(填序号)
A.属于同素异形体
B.因为晶体结构不同而导致性质有差别
C.黄铁矿比白铁矿更稳定
(3)反应Ⅲ制取 S22-时,溶液必须保持为碱性,除了S2- 与酸反应外,还有更重要的原因是(用离子方程式表示)___________________________.
(4)室温下,Li/FeS2 二次电池所用的电解质是非水液体电解质,放电行为与温度有关。
①该电池电解质为非水液体电解质,原因是____________________________________.
②温度低时,锂与FeS2反应只生成A物质,产生第一次放电行为;温度升高,锂与A继续反应(产物之一为Fe),产生第二次放电行为。若二次行为均进行完全且放电量恰好相等。请写出化学反应方程式:
第一次放电:__________________;第二次放电:__________________________。
(5)制取高纯度黄铁矿的另一种方法是:以LiCl- KC1低共熔点混合物为电解质,FeS为阳极,Al为阴极,在适当的电压下电解。写出阳极反应式___________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期三调考试化学试卷(解析版) 题型:选择题
下列说法或解释不正确的是
A.等物质的量浓度的下列溶液中,
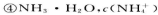 由大到小的顺序是①>②>③>④
由大到小的顺序是①>②>③>④
B.室温下,向0. 01 mol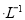 NH4HSO4溶液中滴加NaOH溶液至中性:
NH4HSO4溶液中滴加NaOH溶液至中性:
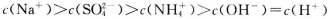
C.向0.2 mol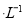 NaHCO3溶液中加入等体积0.1 mol
NaHCO3溶液中加入等体积0.1 mol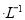 NaOH溶液:
NaOH溶液:
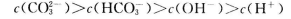
D.物质的量浓度均为1 mol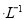 的NaCl和MgCl2混合液1L中,含有Cl-的数目为3
的NaCl和MgCl2混合液1L中,含有Cl-的数目为3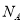 (
(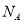 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期期中考试理综化学试卷(解析版) 题型:选择题
25 ℃时,关于①O.l mol·L-1的NH4Cl溶液②0.1 mol·L-1的NaOH溶液,下列叙述正确的是
A.若向①中加适量水,溶液中c(Cl-)/c(NH4+ )的值减小
B.若向②中加适量水,水的电离平衡正向移动
C.若将①和②均稀释100倍,①的pH变化更大
D.若将①和②混合,所得溶液的pH=7,则溶液中的c(NH3·H2O)>c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三4月阶段测试理综试卷化学试卷(解析版) 题型:简答题
(15分)用NH3催化还原NxOy可以消除氮氧化物的污染。
已知:反应I:4NH3(g)+6NO(g)  5N2(g)+6H2O(l) △H1
5N2(g)+6H2O(l) △H1
反应II:2NO(g)+O2(g)  2NO2(g) △H2 (且|△H1| =2|△H2|)
2NO2(g) △H2 (且|△H1| =2|△H2|)
反应III:4NH3(g)+6NO2(g)  5N2(g)+3O2(g)+6H2O(l) △H3
5N2(g)+3O2(g)+6H2O(l) △H3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
298 | K1 | K2 | |
398 | K1′ | K2′ |
(1)推测反应III是 反应(填“吸热”或“放热”)
(2)相同条件下,反应I在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。
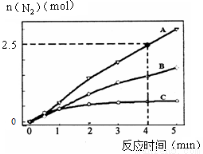
①计算0~4分钟在A催化剂作用下,反应速率v(NO)= 。
②下列说法正确的是 。
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(3)一定条件下,反应II达到平衡时体系中n(NO) ∶n(O2)∶n(NO2)=2∶1∶2。在其它条件不变时,再充入NO2气体,分析NO2体积分数——φ(NO2)的变化情况:(填“变大”、“变小”或“不变”)恒温恒压容器,φ(NO2) ;恒温恒容容器,φ(NO2) 。
(4)一定温度下,反应III在容积可变的密闭容器中达到平衡,此时容积为3 L,c(N2)与反应时间t变化曲线X如下图所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z。则:

①变为曲线Y改变的条件是 。变为曲线Z改变的条件是 。
②若t2降低温度,t3达到平衡,请在上图中画出曲线X在t2- t4内 c(N2)的变化曲线。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省金华十校高三下学期高考模拟(4月)理综化学试卷(解析版) 题型:选择题
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且原子的最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A.原子半径:W>Z>Y>X>M
B.XZ2、X2M2、W2Z2均为直线型的共价化合物
C.由X元素形成的单质不一定是原子晶体
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键、又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气是一种新型的绿色能源,又是一种重要的化工原料.
合成氨反应的热化方程式如下:
N2(g)+3H2(g)⇌2NH3(g);△H=﹣92.4kJ/mol
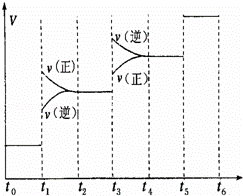
(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.
图中t1时引起平衡移动的条件可能是 ,
其中表示平衡混合物中NH3的含量最高的一段时间是 ,若t0﹣t1,t1﹣t3,t3﹣t5这三段平衡常数分别用K1,K2,K3表示,那么K1,K2,K3的大小关系是
(2)若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂反应的△H (填“增大”、“减小”或“不改变”).
(3)温度为T℃时,将2a mol H2和 a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com