
| X | Y | ||
| Z | W | ||
| T |
| A. | 元素X、W、Z在自然界中均可以游离态存在 | |
| B. | 元素X、Y、W的原子半径依次递增 | |
| C. | 实验室储存T的单质时,应在其表面覆盖少量的水 | |
| D. | 元素Z的氧化物是制作计算机芯片的材料 |
分析 X、Y、Z、W为短周期元素,由元素周期表可知:X应位于第二周期,且应处于周期表中右半部分,W与Y处于同一主族,且W元素原子的核电荷数为Y元素的2倍,则Y为O元素,W为S元素,X为N元素,Z为Si元素,T为Br元素,据此结合选项判断即可.
解答 解:X、Y、Z、W为短周期元素,由元素周期表可知:X应位于第二周期,且应处于周期表中右半部分,W与Y处于同一主族,且W元素原子的核电荷数为Y元素的2倍,则Y为O元素,W为S元素,X为N元素,Z为Si元素,T为Br元素,
A.Si元素是亲氧元素,在自然界中以硅酸盐和氧化物的形式存在,没有单质,故A错误;
B.X为N元素,Y为O元素,W为S元素,原子半径:S>N>O,故B错误;
C.T为Br元素,实验室储存Br的单质时,应在其表面覆盖少量的水,防止液溴挥发,故C正确;
D.Z为Si元素,硅单质是制作计算机芯片的材料,故D错误;
故选C.
点评 本题考查元素的位置与性质、结构的关系,难度不大,解题是时注意元素的性质的递变规律及其应用,把握元素在周期中的位置是解题的关键,侧重于考查学生的分析能力和应用能力.


科目:高中化学 来源: 题型:选择题
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-55.6 kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-55.6 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6 kJ•mol-1 | |
| D. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-889.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 试剂 | 乙醚 | 乙醇 | 甲酸 | 甲酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 100.5 | 54.4 |
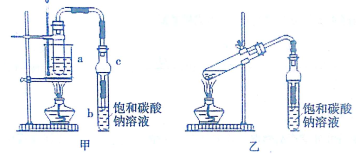
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
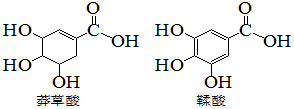
| A. | 莽草酸分子式为C7H10O5 | |
| B. | 两种酸都能与溴水发生加成反应 | |
| C. | 鞣酸分子与莽草酸分子互为同系物 | |
| D. | 等物质的量的两种酸与足量氢氧化钠反应,消耗氢氧化钠的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
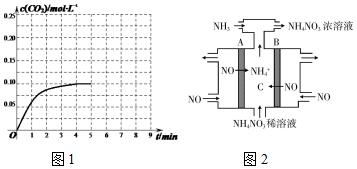 2016年10月11日,神舟十一号飞船搭乘CZ-2F火箭成功发射.在重达495 吨的起飞重量中,95%的都是化学推进剂.
2016年10月11日,神舟十一号飞船搭乘CZ-2F火箭成功发射.在重达495 吨的起飞重量中,95%的都是化学推进剂.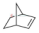 (C7H10)是一种重要的高密度液体燃料化学推进剂.已知:
(C7H10)是一种重要的高密度液体燃料化学推进剂.已知:| 燃料 | 密度(g•cm-3) | 体积热值(J•L-1) |
| 降冰片烯 | 1.0 | 4.2×107 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1mol•L-1的Na2A溶液中,c(A2-)+c(HA-)+2c(Na+)=0.5mol•L-1 | |
| B. | 在0.1mol•L-1的H2A溶液中,c(H+)>0.12mol•L-1 | |
| C. | 将同浓度(0.1mol•L-1)的NaHA和Na2A溶液等体积混合,混合溶液可能呈碱性 | |
| D. | 0.1mol•L-1的NaHA溶液中离子浓度为c(Na+)>c(H+)>c(A2-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ•mol-1) | 436 | 157 | 568 | 432 | 298 |
| A. | 432kJ•mol-1>E(H-Br)>298kJ•mol-1 | B. | H2(g)+F2(g)=2HF(g)△H=25kJ•mol-1 | ||
| C. | 表中最稳定的共价键是H-F | D. | H2(g)→2H(g)△H=+436kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
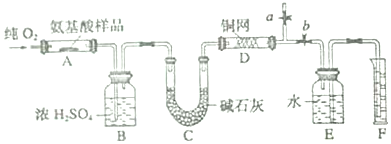
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com