
�Ƽ������[KNH4Fex(SO4)y(OH)z]������ˮ��ϡ���ᣬ��ȡ�Ƽ���������������£�

��1����ҺX�� �� ��
��2��������Һ���Ƿ����K���IJ����� �� ��
��3���Ƽ�������Ļ�ѧʽ��ͨ������ʵ��ⶨ��
�ٳ�ȡһ����������Ʒ����ϡ�������ܽ⣬��������Һת��������ƿ�����Ƴ�100.00 mL��ҺA��
����ȡ25.00 mL��ҺA�����������ữ��BaCl2��Һ��������ȫ�����ˡ�ϴ�ӡ����������أ��õ���ɫ����9.32 g��
����ȡ25.00 mL��ҺA����������NaOH��Һ�����ȣ��ռ�����״��������224mL��ͬʱ�к��ɫ�������ɡ�
�ܽ���������ó������ˡ�ϴ�ӡ����գ����յù���4.80 g��
ͨ������ȷ���Ƽ�������Ļ�ѧʽ(д���������)��
��
��1����ˮ����д��NH3��H2O������2�֣�
��2���ýྻ�IJ�˿(����˿)պȡ��Һ�ھƾ��ƻ��������գ�����ɫ���ܲ����۲죨1�֣������������ɫ�������K����1�֣�
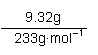 |
��3��n(SO )��n(BaSO4)�� ��0.04 mol ��1�֣�
)��n(BaSO4)�� ��0.04 mol ��1�֣�
 |
n(NH )��n(NH3)�� ��0.01 mol ��1�֣�
)��n(NH3)�� ��0.01 mol ��1�֣�
 |
n(Fe3��)��2n(Fe2O3)��2�� ��0.06 mol ��1�֣�
n(K��)��n(NH )��0.01 mol ��1�֣�
)��0.01 mol ��1�֣�
���ݵ���غ㣺n(OH��)��n(K��)��n(NH )��3n(Fe3��)��2n(SO
)��3n(Fe3��)��2n(SO )��0.12 mol��2�֣�
)��0.12 mol��2�֣�
n(K��)��n(NH )��n(Fe3��)��n(SO
)��n(Fe3��)��n(SO )��n(OH��)��1��1��6��4��12 ��1�֣�
)��n(OH��)��1��1��6��4��12 ��1�֣�
�Ƽ�������Ļ�ѧʽΪKNH4Fe6(SO4)4(OH)12 ��1�֣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NaI��NaBr�Ļ����Һ��ͨ����������������ַ�Ӧ����Һ���ɣ�����������������õ���������
A��NaCl��I2 B.NaCl��NaBr C��NaBr��I2 D��NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ���������������أ�����˵���������
A����ʳ����ľ�һ���¶����ܷ���ʱ��Խ����ζԽŨ������Ϊ��������
B����ά���������ڿ�ˮ��Ϊ�����ǣ��ʿ�ֱ�ӳ�Ϊ�����Ӫ������
C���ô����Ʋ�����������ʯ�������õ��۷��ͷ������ƾ��������CO2
D���ý��ݹ����������Һ�Ĺ���������ˮ���ͷŵ���ϩ���ɴﵽˮ�����ʵ�Ŀ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA Ϊ�����ӵ�������ֵ������˵����ȷ����
A����״���£�11.2 L NO��11.2 L O2��Ϻ�����ķ�������ΪNA
B����״���£�2.24LCl2ͨ������H2O��NaOH��Һ��ת�Ƶĵ�������Ϊ0.1NA
C��0.1mol�İ��ף�P4�������Ȼ�̼��CCl4���������Ĺ��ۼ�����Ϊ0.4NA
D���ھ���ͭ����ͭ�Ĺ����У�����������ͭ32gת�Ƶ�������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������������
A��NaHCO3��Һ�У�c(H+) +c(H2CO3)��c(CO32��) +c(OH��)
B��25��ʱ��0.2mol��L��1����������0.05 mol��L��1Ba(OH)2��Һ��Ϻ���Һ��pH��1
C��pH��3�Ķ�Ԫ����H2R��Һ��pH��11��NaOH��Һ��Ϻ��Һ��pH����7��
��Ӧ��Ļ��Һ�У�2c(R2��)+c(HR��)��c(Na��)
D��25��ʱ����0.3 mol��L��1 HY��Һ��0.3 mol��L��1 NaOH��Һ�������Ϻ���Һ��pH��9����c(OH��)��c(HY)��c(H+)��1��10��9 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���������
A�������ڻ�ѧ��Ӧ�п����ٷ֣�ԭ���ڻ�ѧ��Ӧ�в����ٷ�
B������������������ԣ���ԭ�������������
C�����塢��Һ����Һ��Ϊ��������ʡ��ǵ���ʾ�Ϊ������
D��12C��13C��14CΪ̼Ԫ�ص����ֺ��أ����ʯ��ʯī��Ϊͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Դ�Ŀ������������������Ŀɳ�����չϢϢ��أ�����������ú���Դ�ǰ���������ǰ���ش���⡣
I����֪��Fe2O3��s��+3C��ʯī��=2Fe��s��+3CO��g����H= a kJ•mol-1
CO��g��+1/2O2��g��=CO2��g����H= b kJ•mol-1
C��ʯī��+O2��g��=CO2��g����H= c kJ•mol-1
��Ӧ��4Fe��s��+3O2��g��=2Fe2O3��s�����ʱ��H= kJ•mol-1
��1������ԭ��صĹ���ԭ�������л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
A��C��s��+CO2��g��= 2CO��g��
B��NaOH��aq��+HCl��aq��= NaCl��aq��+H2O��l��
C��2H2O��l��= 2H2��g��+O2��g��
D��CH4��g��+2O2��g��= CO2��g��+2H2O��l��
����KOH��ҺΪ�������Һ��������ѡ��Ӧ������Ƴ�һ��ԭ��أ���д����ԭ��صĵ缫��Ӧ
������
������
 ��2���������ȣ�ClO2����һ�ָ�Ч��ȫ������ˮ��������ClO2��һ�ֻ���ɫ���壬������ˮ��ʵ������NH4Cl�����ᡢNaClO2Ϊԭ���Ʊ�ClO2�������£�
��2���������ȣ�ClO2����һ�ָ�Ч��ȫ������ˮ��������ClO2��һ�ֻ���ɫ���壬������ˮ��ʵ������NH4Cl�����ᡢNaClO2Ϊԭ���Ʊ�ClO2�������£�
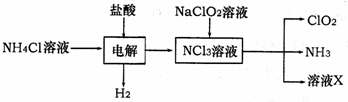
��֪���������з����ķ�ӦΪ��
NH4Cl+2HCl NCl3+3H2��������NCl3�е�Ԫ��Ϊ+3�ۣ�
��д�����ʱ�����ĵ缫��Ӧʽ
�����ĵ缫��Ӧʽ
���������Ϸŵ�����ʣ������ӣ���
�۳�ȥClO2�е�NH3��ѡ�õ��Լ��� ������ţ�
A����ʯ�� B����ʯ�� C��ŨH2SO4 D��ˮ
�������������У�ÿ����1mol ClO2�������� mol NCl3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���»�ѧ������ȷ����
A���������ʽ C6H6 B���Ҵ��ķ���ʽCH3CH2OH
C����ϩ�Ľṹ��ʽCH2CH2 D����ȩ�Ľṹʽ�� 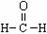
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��M��WΪ���ֶ�����Ԫ�ء�X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��X��Z���γ�XZ2���ӣ�Y��M�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ0.76g/L��W����������X��Y��Z��M����Ԫ��������֮�͵�1/2������˵����ȷ���ǣ� ��
A��ԭ�Ӱ뾶��W��Z��Y��X��M
B��XZ2��M2Z2��W2Z2��Ϊ���Ǽ��Լ��Ĺ��ۻ�����
C����XԪ���γɵĵ����еĿ��Ե���
D����X��Y��Z��M����Ԫ���γɵĻ������в����ܺ������Ӽ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com