
【题目】如图所示与对应叙述相符的是![]()

A.图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则![]()
B.图乙表示![]() 的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸
的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸![]() 乙酸
乙酸
C.图丙是用![]() 0
0![]() 溶液滴定
溶液滴定![]() mL盐酸的滴定曲线
mL盐酸的滴定曲线
D.图丁表示反应![]() 平衡时
平衡时![]() 体积分数随起始
体积分数随起始![]() 变化的曲线,则转化率:
变化的曲线,则转化率:![]()
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为同一周期原子序数依次增大的短周期主族元素,已知A、B、D三种原子最外层共有10个电子,且这三种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的核电荷数是最外层电子数的3倍。
(1)A的单质在空气中燃烧的产物为____填化学式)。
(2)D、E的最高价氧化物的水化物的酸性比较:_______ (用化学式表示)。
(3)元素E形成的单质通入D的一种氧化物的水溶液中发生反应,生成两种常见的强酸。该反应的化学方程式为____。
(4)写出B、A两元素的最高价氧化物的水化物相互反应的离子方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
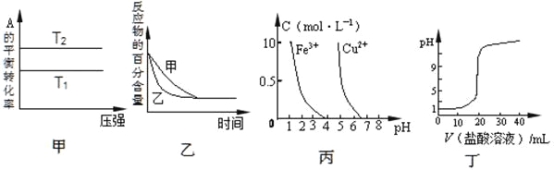
A.由图甲可以判断:若T1>T2,反应A(g)+ B(g)![]() 2C(g)的△H<0
2C(g)的△H<0
B.图乙表示压强对可逆反应2A(g)+2 B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4
D.图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,溶液pH随加入盐酸体积的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种主族元素(过渡元素略去)在周期表中的位置如下:
A | |||||||
M | B | D | |||||
E | G | R | J | ||||
T | |||||||
(1)E、G、T的原子半径由大到小的顺序是_____(填元素符号)。
(2)硒元素(34Se)与D同主族,其非金属性比D______(填“强”或“弱”)。
(3)E、G元素最高价氧化物对应水化物之间能反应,离子方程式为:_______。
(4)E、D两元素能形成原子个数比1:1 型化合物的电子式为________。
(5)A与M形成的分子可能是________(填字母序号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,浓度均为0.1 mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A.酸性强弱:H2CO3>HF
B.①和②中溶质均未水解
C.离子的总浓度:①>③
D.④中:c(HCO3-) + 2c(CO32-) + c(H2CO3)![]() 0.1 mol/L
0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中的某些元素之间存在着特殊的“对角线关系”,例如:![]() 、
、![]() 、
、![]() 相似等,下列说法不正确的是
相似等,下列说法不正确的是![]()
A.氢氧化铍是两性氢氧化物
B.B、Si的电负性数值相似
C.Li和Mg的原子半径相近,且核外电子排布相近
D.Li在![]() 中燃烧能生成
中燃烧能生成![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的叙述正确的是
A.在硅酸钠溶液中滴入稀盐酸,溶液变浑浊,说明Cl元素的非金属性强于Si元素
B.Zn与稀硫酸反应时,滴加少量CuSO4溶液,反应速率加快,说明CuSO4在该反应中起催化剂作用
C.用酚酞作指示剂,盐酸滴定Na2CO3溶液,达到滴定终点时,离子浓度关系为:![]()
D.将NaAlO2溶液与NaHCO3溶液混合,出现白色沉淀,是两种溶液水解相互促进的结果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是中学化学常见的三种物质,它们之间的相互转化关系如下![]() 、Y、Z、E、F为英文字母,部分反应条件及产物略去
、Y、Z、E、F为英文字母,部分反应条件及产物略去![]()

I.若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
(1)则Y和新制氯水主要成分反应生成两种强酸的化学方程式______________。
(2) Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为________________。
(3)Z的水溶液可以制得某种强酸E。实验室用![]() 的浓
的浓![]() 溶液配制
溶液配制![]() 稀E溶液
稀E溶液![]() 。
。
①制该稀E溶液需要使用的玻璃仪器有胶头滴管、量筒、烧杯、____和_____;
②算所需E浓溶液的体积为___mL(保留1位小数)。
II.若Z是淡黄色固体粉末。在呼吸面具或潜水艇中由Z和CO2制备氧气的化学反应方程式为____。
III.若Z是红棕色气体。
(1)试写出Z与水反应制备另一种强酸F的化学方程式_______。
(2)2.0g铜镁合金完全溶解于![]() 密度为
密度为![]() 质量分数为
质量分数为![]() 的浓F溶液中,得到Z和
的浓F溶液中,得到Z和![]() 和
和![]() 均为浓F溶液的还原产物
均为浓F溶液的还原产物![]() 的混合气体
的混合气体![]() 标准状况
标准状况![]() ,向反应后的溶液中加入
,向反应后的溶液中加入![]() 溶液,当金属离子全部沉淀,得到
溶液,当金属离子全部沉淀,得到![]() 沉淀。则合金中铜与镁的物质的量之比为_____,加入NaOH溶液的体积为_____mL。
沉淀。则合金中铜与镁的物质的量之比为_____,加入NaOH溶液的体积为_____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )

A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com