
����Ŀ��pC������pH����ָ��ϡ��Һ�е�����Ũ�ȵij��ö����ĸ�ֵ����ij��Һ��ij���ʵ�Ũ��Ϊ1��10��3mol/L�������Һ�и����ʵ�pC����lg(1��10��3)��3����ͼΪ25��ʱH2CO3��Һ��pC��pHͼ(������Ũ��С��10-5mol/L������Ϊ�����Ӳ�����)������˵������ȷ����

A��ij�¶��£�CO2������Һ��Ũ����0.05 molL��1������1/5��CO2ת��ΪH2CO3������ʱ��Һ��pHԼΪ5���ݴ˿ɵø��¶���CO2������Һ��H2CO3�ĵ����Ϊ0.1% ��
B��25��ʱ��H2CO3һ������ƽ�ⳣ������ֵKa1=10��6
C����Na2CO3��Һ�еμ�������pH����11ʱ����Һ�У�c(Na+)+c(H+)=2c(CO32��)+c(OH��)+c(HCO3��)
D��25��ʱ��0.1mol/LNa2CO3��c(HCO3��)��0.1mol/LH2CO3��c(HCO3��)��
���𰸡�C
��������
���������A��CO2������Һ��Ũ����0.05mol/L������1/5��CO2ת��ΪH2CO3��pH=5��c(H+)=10-5mol/L�����H2CO3�ĵ����Ϊ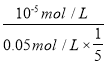 ��100%=0.1%����A��ȷ��B����ͼ���֪��pH=6ʱ��pC(H2CO3)=pC(HCO3-)�����Ka1(H2CO3)=
��100%=0.1%����A��ȷ��B����ͼ���֪��pH=6ʱ��pC(H2CO3)=pC(HCO3-)�����Ka1(H2CO3)=![]() =
=![]() =10-6����B��ȷ��C����Na2CO3��Һ�еμ�������pH����11ʱ�����ݵ���غ㣬c(Na+)+c(H+)=2c(CO32��)+c(OH��)+c(HCO3��)+c(Cl-)����C����D������ͼ��Na2CO3��һ��ˮ�ⳣ��ԼΪ10-3��H2CO3��һ�����볣��ԼΪ10-4.7�����0.1mol/LNa2CO3��c(HCO3��)��0.1mol/L��c(HCO3��)��D��ȷ����ѡC��
=10-6����B��ȷ��C����Na2CO3��Һ�еμ�������pH����11ʱ�����ݵ���غ㣬c(Na+)+c(H+)=2c(CO32��)+c(OH��)+c(HCO3��)+c(Cl-)����C����D������ͼ��Na2CO3��һ��ˮ�ⳣ��ԼΪ10-3��H2CO3��һ�����볣��ԼΪ10-4.7�����0.1mol/LNa2CO3��c(HCO3��)��0.1mol/L��c(HCO3��)��D��ȷ����ѡC��


 �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д� �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��ǰ������ԭ�������������������Ԫ�ء�AԪ��ԭ�ӵĺ����������������Ӳ�����BԪ�ػ�̬ԭ���������ܼ��Ҹ��ܼ���������ͬ��A��D���γ����ֳ���Һ̬������G��H����ԭ����֮�ȷֱ�Ϊ1��1��2��1��EԪ��ԭ�ӵ�K��L�������֮�͵�����M��N�������֮�͡���ش����и���(�漰Ԫ��������Ӧ��ѧ���ű�ʾ)��
��1��BCD����Ԫ���е縺������Ԫ�����̬ԭ�ӵĵ����Ų�ͼΪ____________��
��2������һ���ռ��˶�״̬�ĵ�����ԭ�Ӻ�����ֵĸ����ܶȷֲ�����____________������������B�Ļ�̬ԭ���У��������____________�������෴�ĵ��ӡ�
��3����E��D�γɵľ�����ͼ1��ʾ��������E2+��Χ�Ⱦ��������E2+��______����ED����ɫ��ӦΪש��ɫ��������������ǵĻ����ﶼ���Է�����ɫ����Ӧ����ԭ����____________��E��B���γɵľ���ľ����ṹ��NaCl���������(��ͼ2��ʾ)�����þ����к��е�������B22-�Ĵ��ڣ�ʹ������һ������������������E2+����λ��Ϊ_______���û�����ĵ���ʽΪ_______��

��4���ø�����������Һ̬Hʱ��һ��H�������ͷų�һ�����ӣ�ͬʱ����һ�������ӡ����ͷų����ĵ��ӿ��Ա�����H�����γɵġ�������������ΪH���Ӽ����γɡ�������ԭ��____________��
����H�����ͷų�����ʱ������һ�������Ӿ��н�ǿ�������ԣ���д������������SO2��ˮ��Һ���� Ӧ�����ӷ���ʽ________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��A��B��C��D��E��ԭ����������������Ԫ��������Ϣ�����
Ԫ�ر�� | Ԫ��������Ϣ |
A | ������ۺ�����۵ľ���ֵ֮��Ϊ2 |
B | ��Eͬ���� |
C | lmo1C����������ˮ��Ӧ���ڱ�״��������11.2LH2 |
D | ԭ�������������������������� |
E | ��һ�������ӵĵ��Ӳ�ṹ��Arԭ����ͬ |
��1�� A�����ڱ��е�λ��Ϊ ��
��2��B��C�γɵĻ�����ĵ���ʽΪ ��
��3��B��D�����ӵİ뾶��СΪ ��
��4��Ԫ�طǽ�����ǿ���Ƚ��кܶ��������B��E�ķǽ�����ǿ�����о������в����е��� (�����)��
A���Ƚ����ֵ��ʵ���ɫ
B���Ƚ����ֵ�����H2���ϵ����׳̶�
C��������Ԫ�������ڱ��е�λ��
D���Ƚ϶�Ӧ�����ӵĻ�ԭ��
e.�Ƚ�����������Ӧˮ���������
��5��EԪ��������������Ԫ���е�һ��Ԫ���γɹ��ۻ���������е�ԭ�Ӹ�����Ϊ1��3����Է�������Ϊ120.5��������ʵĻ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ա���ȩΪԭ���Ʊ����屽��ȩ(ʵ��װ�ü�ͼ��������ʵķе������)����ʵ�鲽��Ϊ��
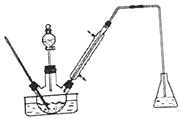
����1:������ƿ�е�һ����ȵ���ˮAlCl3�� 20mLl�� 2 -���������20mL����ȩ��ֻ�Ϻ�.������60���������μӾ�H2SO4�������Һ��20mL�����·�Ӧһ��ʱ�䣬��ȴ��
����2:����Ӧ����ﻺ������һ������ϡ�����У�__________��
����3:�л�����10%NaHCO3��Һϴ�ӡ���ϴ�ӵ��л������������ˮMgSO4���壬����һ��ʱ�����ˡ�
����4:��ѹ�����л��࣬�ռ���Ӧ��֡�
��1��ʵ��װ���������ܵ���Ҫ������__________����ƿ�е���ҺӦΪ__________��
��2������1������������У�AlCl3�Ǵ��������Ʋ�1�� 2-�������������__________��
��3����ͬѧ���齫װ�����¶ȼƻ��ɽ���������ô�¶ȼ�Ӧ�Ƶ�ʲô�ط�__________��
��4������2����������__________��
��5������3����10%��NaHCO3��Һϴ�ӵľ��������__________��������ˮMgSO4�����������__________��
��6������4�в��ü�ѹ����������Ϊ�˷�ֹ__________��
��7������ռ������屽��ȩ10mL�����ʵ��IJ���Ϊ__________��
����������ʵķе�(101kPa)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���224L HCl��������635mLˮ�У�����������ܶ�Ϊ1.18gcm-3���Լ��㣺
��1��������������ʵ���Ũ����_________��
��2��ȡ����������10mL��ϡ����118mL������ϡ��������ʵ���Ũ����_________��������Ͳȡ10mL����ʱ���ӣ�������������ȷ����ϡ����Ũ��_________(����ƫ������ ������������ƫС��)��
��3����40.0mL 0.065molL-1 Na2CO3��Һ�У�������2����ϡ�͵�ϡ���ᣬ�ӱ�����ʹ��Ӧ������CO2���壬����ϡ��������������_________ mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����16�֣�����β���е���Ҫ��Ⱦ����NO��CO��Ϊ���������Ⱦ���������ͨ�����·�Ӧ����������β����
��1��2NO��g��+2CO��g��2CO2��g��+N2��g����H=��746.5KJ/mol ������Ϊʹ�ô�����
��֪��2C ��s��+O2��g��2CO��g����H=��221.0KJ/mol
C ��s��+O2��g��CO2��g����H=��393.5KJ/mol
��N2��g��+O2��g��=2NO��g����H= kJmol��1��
��2��T���£���һ�ݻ�������ܱ������У�ͨ��һ������NO��CO�������崫������ò�ͬʱ��NO��CO��Ũ�����±�
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 | |||||||
C��NO��10��4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 | |||||||
C��CO��10��3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 | |||||||
��C2��������ֵΪ ������ĸ��ţ���
A��4.20 B��4.00 C��2.95 D��2.80
��3������ͬ���ʵ�����H2O��g����CO��g���ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У����з�Ӧ��H2O��g��+CO��g��CO2��g��+H2��g�����õ������������ݣ�
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
H2O | CO | CO | H2 | |||
i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
iii | 900 | a | b | c | d | t |
��a=2��b=1����c= ����ƽ��ʱʵ����ii��H2O��g����ʵ����iii��CO��ת���ʵĹ�ϵΪ��ii��H2O�� ��iii��CO�������������������=������
��4���������������Դ����CO�ڴ����������Ʊ������ѵķ�Ӧԭ��Ϊ��2CO��g��+4H2��g��CH3OCH3��g��+H2O��g������֪һ�������£��÷�Ӧ��CO��ƽ��ת�������¶ȡ�Ͷ�ϱ�![]() �ı仯������ͼ1��ʾ��
�ı仯������ͼ1��ʾ��
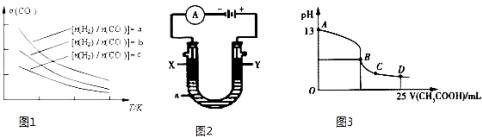
��a��b��c���Ӵ�С��˳������Ϊ ��
������ͼ������жϸ÷�ӦΪ���ȷ�Ӧ�������� ��
��5��CO�����Ĵ������ɲⶨ����β���Ƿ�����ŷű����÷����ǵĹ���ԭ��������ȼ�ϵ�أ����е�����������ƣ�Y2O3��������ﯣ�ZrO2�����壬�ܴ���O2����
�����ĵ缫��ӦʽΪ ��
�����������Ϊ��Դ��ͨ���������ӳ�ͼ2����X��YΪʯī��aΪ2L 0.1mol/L KCl��Һ���һ��ʱ���ȡ25mL �����������Һ���μ�0.4mol/L����õ�ͼ3���ߣ�������������ʧ����������ˮ����Һ����仯���Բ��ƣ�������ͼ�����㣬������������ ����һ����̼������Ϊ g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʾ��Ԫ�����ڱ�ʾ��ͼ��һ���֣����ݱ���10��Ԫ�أ���Ԫ�ط��Ż�ѧʽ��ա�
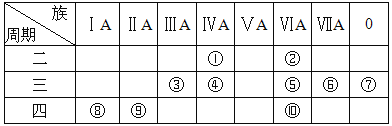
��1��������Ԫ����,��������ǿ���� (��Ԫ�ط���)����ѧ��������õ��� (��Ԫ�ط���)��
��2��������Ԫ����,����������Ӧ��ˮ��������Ե�Ԫ���� (��Ԫ�ط���)����ˮ������NaOH��Һ��Ӧ�����ӷ���ʽΪ ��
��3��������Ԫ����,����������Ӧ��ˮ�����������ǿ���� (�ѧʽ)��������ǿ���� (�ѧʽ)��
��4�������������������γɵļ����ӵİ뾶�ɴ�С��˳���� ���������ӷ��ţ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ�����ݻ�Ϊ2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ����ͼ�����ݷ�����
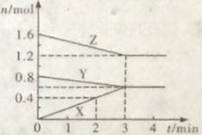
��1���÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2����Ӧ��ʼ��2minĩ�� X�ķ�Ӧ����Ϊ ��
��3����Ҫ�ӿ�÷�Ӧ�Ļ�ѧ��Ӧ���ʿ��Բ�ȡ�Ĵ�ʩ�У���������Ũ�ȡ���ѹ�� ��ʹ���������ȡ�
��4����Ӧ�ﵽƽ��״̬����ʼʱ��Ϊ min,ƽ��ʱZ��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1����֪��2SO2(g)��O2(g) ![]() 2SO3(g) ��H����196.6 kJ/mol
2SO3(g) ��H����196.6 kJ/mol
2NO(g)��O2(g) ![]() 2NO2(g) ��H����113.0 kJ/mol
2NO2(g) ��H����113.0 kJ/mol
��ӦNO2(g)��SO2(g) ![]() SO3(g)��NO(g)�Ħ�H��________ kJ/mol��
SO3(g)��NO(g)�Ħ�H��________ kJ/mol��
��2��һ�������£���NO2��SO2�������1��2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����________��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ��� d��ÿ����1 mol SO3��ͬʱ����1 mol NO2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com