
【题目】下列关于各装置图的叙述,不正确的是
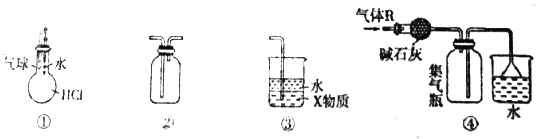
A. 装置①可验证HCl气体在水中的溶解性
B. 装置②可用于收集H2、Cl2、NO2、NO等气体
C. 装置③中X为四氯化碳时,可用于吸收氨气或氯化氢
D. 装置④可用于干燥、收集并吸收多余的氨气
【答案】B
【解析】A.HCl极易溶于水,挤压胶头滴管,瓶内气体减少;B.NO能与空气中的氧气反应生成二氧化氮,不能用排空气法收集;C.四氯化碳在下层,可起防止倒吸的作用;D.氨气与碱石灰不反应,且氨气的密度比空气密度小。
A.HCl极易溶于水,挤压胶头滴管,瓶内气体减少,则气球变大可说明HCl气体在水中的溶解性,选项A正确;B.NO能与空气中的氧气反应生成二氧化氮,不能用排空气法收集,选项B不正确;C.四氯化碳在下层,可起防止倒吸的作用,则装置③可用于吸收氨气或氯化氢,选项C正确;;
D.氨气与碱石灰反应,且氨气的密度比空气密度小,则能利用碱石灰干燥,且收集方法合理,选项D正确。答案选B。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | F | H | I |
(1)表中元素,化学性质最不活泼的是____,只有负价而无正价的是______,还原性最强的单质是______,氧化性最强的单质是___。
(2)最高价氧化物的水化物中,既能和盐酸又能和氢氧化钠反应的是___,酸性最强的是____,碱性最强的是_____。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的_____。
(4)在A、B、C、D、E、F、G、H中,原子半径最大的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,其目的是_________________________________________________。
(2)FeCl3净水的原理是(用离子方程式表示):______________________________将AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_________ 。
(3)用纯碱溶液可清洗油污,其原因是(用离子方程式表示):_________________________
(4)泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈现碱性的原因是(用离子方程式表示)______;灭火器内另一容器中装有Al2(SO4)3溶液,该溶液呈酸性的原因是(用离子方程式表示):_________________________,当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧产生的烟气含有的SO2,是大气主要污染物之一。减少煤燃烧对大气造成的污染,应从多方面采取措施。
(1)在煤燃烧前需对煤进行脱硫处理。
①一种烟气脱硫技术是向煤中加入适量石灰石,可大大减少燃烧产物中SO2的含量,最后生成CaSO4,该反应的化学方程式为_________________________________________。
②煤炭中以FeS2(铁元素为+2价)形式存在的硫,可以采用微生物脱硫技术脱去,其原理如图所示:
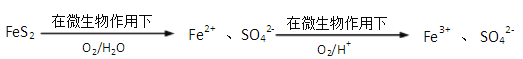
1mol FeS2完全转化为Fe3+ 和SO42-时,FeS2与O2物质的量之比为_____________。
(2)燃煤后烟气脱硫方法之一是利用天然海水的碱性吸收烟气中SO2并转化为无害的SO42-,其流程的示意图如下:
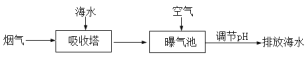
①海水中碳元素主要以HCO3-的形式存在。用离子方程式表示海水呈碱性的原因:_____________。
②研究表明,进入吸收塔的海水温度越低,SO2的脱除效果越好,主要原因是_____________。
③从吸收塔排出的海水呈酸性,并含有较多的HSO3-,排入曝气池进行处理时,需要鼓入大量空气。空气的作用是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气)。下列说法错误的是
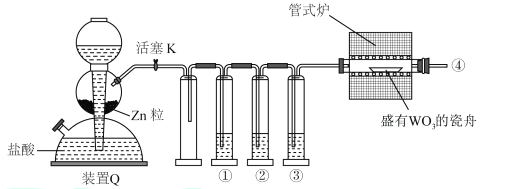
A. ①、②、③中依次盛装KMnO4溶液、焦性没食子酸溶液、浓H2SO4
B. 为保证H2的纯度,装置Q(启普发生器)中的锌粒可以用还原铁粉代替
C. 结束反应时,先停止加热,再关闭活塞K
D. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)玻璃棒是化学实验中常用的仪器之一,其主要用于搅拌、过滤或转移液体时的引流。下列实验过程中,通常不需要使用玻璃棒的是___________(填序号,下同)
①用pH试纸测定Na2CO3溶液的pH
②用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
③实验室中用FeCl3溶液和沸水制取Fe(OH)3胶体
④用已知浓度的稀盐酸滴定未知浓度的氢氧化钠溶液
⑤取某溶液做焰色反应实验,检验该溶液中是否含有钠元素
(2)①下列仪器在使用前一定要检查是否漏液的是______________________。
a.容量瓶 b.冷凝管 c.碱式滴定管 d.长颈漏斗 e.分液漏斗
②检查装置气密性是化学实验中的重要操作之一。不进行气密性检查可能导致的后果是____________。
a.收集不到气体 b.造成环境污染
c.观察到的实验现象有误 d.引发爆炸事故
(3)下图所示装置可用于制备某种干燥的纯净气体。该装置中所盛装的药品正确的是_____________。
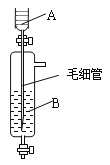
a.A中装浓硫酸,B中装浓盐酸
b.A中装浓盐酸,B中装浓硫酸
c.A中装氢氧化钠浓溶液,B中装浓氨水
d.A中装浓氨水,B中装氢氧化钠浓溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产苯乙烯是利用乙苯的脱氢反应如下,针对上述反应,在其它条件不变时,下列说法正确的是( )

A. 加入适当催化剂,可以提高苯乙烯的产量
B. 在保持体积一定的条件下,充入较多的乙苯,可以提高乙苯的转化率
C. 仅从平衡移动的角度分析,工业生产苯乙烯选择恒压条件优于恒容条件
D. 加入乙苯至反应达到平衡过程中,混合气体的平均相对分子质量不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学要以“研究苯分子的结构”为题目做一次探究活动,下面是其活动记录,请你补全所缺内容。
(1)理论推测:他根据苯的凯库勒式________,推测苯分子中有两种不同的碳碳键,即________和________,因此它能使紫色的________溶液褪色。
(2)实验验证:他取少量的上述溶液加入试管中,然后加入苯,充分振荡,发现_____________________。
(3)实验结论:上述的理论推测是________(填“正确”或“错误”)的。
(4)查询资料:经查阅有关资料,发现苯分子中六个碳原子之间的键________(填“相同”或“不同”),是一种特殊的键,苯分子中的六个碳原子和六个氢原子________(填“在”或“不在”)同一个平面上,应该用________表示苯分子的结构更合理。
(5)发现问题:当他将苯加入溴水中时,充分振荡,发现能使溴水褪色,于是该同学认为所查资料有误。你同意他的结论吗?____。为什么?______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com