
 固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )
固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )| A、只用盐酸一种试剂就可以确定该固体A的成分 |
| B、依次加入Ba(NO3)2溶液、盐酸,若有白色沉淀,则固体A为Na2SO4 |
| C、滴入酸性KMnO4溶液,若KMnO4溶液褪色,则固体A为Na2SO3 |
| D、用pH试纸检验(常温),若pH>7,则固体A可能是Na2CO3 |


科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三者对应的氧化物均为酸性氧化物 |
| B、实验室可用NaOH溶液处理SO2、NO2 |
| C、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D、三者的单质直接与氧气反应都能生成两种氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
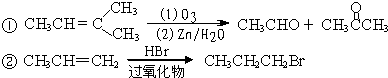
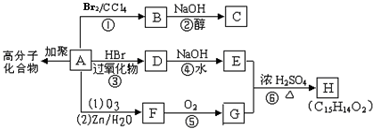
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2?H2的转化率 |
| B、工业上利用电解熔融的氧化铝制取铝,电解熔融的氧化镁制取镁 |
| C、电解精炼铜时,同一时间内阴极溶解铜的质量比阳极析出铜的质量小 |
| D、从海带中提取碘单质的实验中,要经过煅烧、溶解、过滤和萃取等操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:
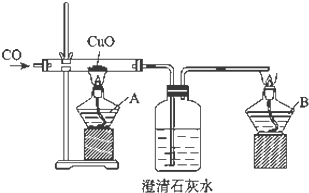 证明CO具有还原性的实验装置,如图所示.
证明CO具有还原性的实验装置,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量固体产物于试管中,加入足量蒸馏水溶解,过滤,分离出不溶固体 | |
| 步骤2:取少量上述不溶固体放入试管中,加入足量CuSO4溶液,充分振荡. | 若固体无明显变化,则假设 |
| 步骤3: | 若溶液基本无色,则假设Ⅰ成立,若溶液呈浅绿色,则假设3成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
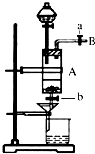 三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl3?6H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,用分液漏斗向A中加过量的盐酸,此时溶液呈浅绿色,再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3?6H2O晶体.
三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl3?6H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,用分液漏斗向A中加过量的盐酸,此时溶液呈浅绿色,再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3?6H2O晶体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com