
| 实验方案(只要求填写选用试剂) | ① | ② |
| 填试剂序号 | 填试剂序号 | |
| 实验现象 | 一支试管中有白色沉淀,另一支试管中先生成白色沉淀,后白色沉淀消失 | 溶液由无色变为黄色(或橙黄) |
| 有关反应的离子方程式 | ①Al3++3OH-═Al(OH)3↓ ②Al(OH)3+OH-═AlO2-+H2O 或③Al3++4OH-═AlO2-+2H2O ④Mg2++2OH-═Mg(OH)2↓ | Cl2+2Br-=2Cl-+Br2 |
| 结论 | 金属性:Mg>Al | 非金属性:Cl>Br |
分析 探索元素的金属性、非金属性的强弱,由①中现象可知,白色沉淀分别为氢氧化镁、氢氧化铝,后氢氧化铝溶解在NaOH溶液中,由最高价氧化物水化物的碱性比较金属性;
比较Cl、Br的非金属性,可利用置换反应,以此来解答.
解答 解:一支试管中有白色沉淀生成,另一支试管中先生成白色沉淀,后白色沉淀消失,说明在MgCl2溶液和AlCl3溶液中分别加入NaOH溶液,由于Al(OH)3具有两性,可溶于NaOH溶液而生成NaAlO2,说明碱性:Ma(OH)2>Al(OH)3,发生离子反应为①Al3++3OH-═Al(OH)3↓、②Al(OH)3+OH-═AlO2-+H2O、或③Al3++4OH-═AlO2-+2H2O、④Mg2++2OH-═Mg(OH)2↓,则金属性:Mg>Al;
比较Cl、Br的非金属性强弱,可用非金属单质与氢气反应的剧烈程度、氢化物的稳定性、对应最高价氧化物的水化物的酸性强弱或非金属之间的置换反应等,由于题中没有氢化物、酸等,则可用非金属之间的置换反应进行验证,即将氯水滴加到NaBr溶液中,观察到溶液由无色变为黄色,说明单质的氧化性:Cl2>Br2,反应的离子方程式为
Cl2+2Br-=2Cl-+Br2,则可说明非金属性:Cl>Br.
故答案为:
| 实验方案(只要求填写选用试剂) | ① | ② |
| ④⑤⑨ | ③⑥ | |
| 实验现象 | 一支试管中有白色沉淀,另一支试管中先生成白色沉淀,后白色沉淀消失 | 溶液由无色变为黄色(或橙黄) |
| 有关反应的离子方程式 | ①Al3++3OH-═Al(OH)3↓ ②Al(OH)3+OH-═AlO2-+H2O 或③Al3++4OH-═AlO2-+2H2O ④Mg2++2OH-═Mg(OH)2↓ | Cl2+2Br-=2Cl-+Br2 |
| 结论 | 金属性:Mg>Al | 非金属性Cl>Br |
点评 本题考查非金属性、金属性的实验探究,题目难度不大,本题注意根据非金属性、金属性的比较角度和所提供的药品进行实验设计.


科目:高中化学 来源: 题型:选择题
| A. | 1mol | B. | 1.33mol | C. | 0.667mol | D. | 0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
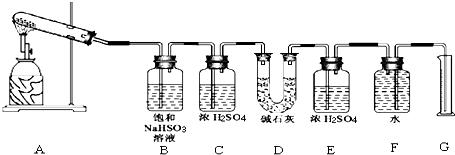
| 实验小组 | 称取CaSO4 的质量(g) | 装置D增加 的质量(g) | 量取气体体积的装置测量的气体体积 (折算成标准状况下气体的体积) (mL) |
| 一 | 4.08 | 2.56 | 224 |
| 二 | 5.44 | 2.56 | 448 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某浓差电池的原理示意如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能.下列有关该电池的说法正确的是( )
某浓差电池的原理示意如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能.下列有关该电池的说法正确的是( )| A. | 电子由X极通过外电路移向Y极 | |
| B. | 电池工作时,Li+通过离子导体移向b区 | |
| C. | 负极发生的反应为:2H++2e-═H2↑ | |
| D. | Y极每生成1 mol Cl2,a区得到2 mol LiCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 参加反应的硝酸是0.92 mol | |
| B. | 合金中镁的质量5.9 g | |
| C. | 反应过程中转移的电子数为0.46 mol | |
| D. | 合金中含有铜0.092 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2 | B. | NaCl | C. | BaSO4 | D. | 葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com