
将22.4g铜和氧化铁的混合物粉末加入到浓度为1 mol•L-1的硫酸中,使之发生反应。
⑴若固体恰好全部溶解,消耗硫酸的体积为V L ,求V的取值范围。
⑵若硫酸溶液过量,反应后溶液的体积为1 L,测得此溶液中Fe2+浓度为0.1 mol•L-1,求原混合物含铜多少克。
⑴0.30≤V<0.42; ⑵3.2g或14.4g
|
⑴有关化学反应为: Fe2O3+3H2SO4=Fe2(SO4)3+3H2O Fe2(SO4)3+Cu=CuSO4+2FeSO4 因此,Fe2O3越多,消耗H2SO4越多,此时,可求得V=0.42L;Fe2(SO4)3与Cu正好完全反应时,消耗H2SO4最少,此时,求得V=0.30 L。 ⑵由Fe2(SO4)3+Cu=CuSO4+2FeSO4, 若Cu完全反应,n(Cu)= 若
|


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:物理教研室 题型:038
常温下,反应
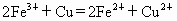 在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.
在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.
(1)若固体恰好全部溶解,消耗硫酸的体积为VL,求V的取值范围.
(2)若硫酸溶液过量,反应后溶液的体积为1L,测得此溶液中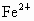 的浓度为0.1mol/L,求原混合物中含铜多少克?
的浓度为0.1mol/L,求原混合物中含铜多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:058
常温下,反应
 在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.
在水溶液中能发生,将22.4g铜和三氧化二铁的混合粉末加入到浓度为1mol/L的硫酸中,使之发生反应.
(1)若固体恰好全部溶解,消耗硫酸的体积为VL,求V的取值范围.
(2)若硫酸溶液过量,反应后溶液的体积为1L,测得此溶液中 的浓度为0.1mol/L,求原混合物中含铜多少克?
的浓度为0.1mol/L,求原混合物中含铜多少克?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com