
| A、大理石、重晶石、光卤石 |
| B、小苏打、苏打、大苏打 |
| C、绿矾、胆矾、明矾 |
| D、铝土矿、硫铁矿、磁铁矿 |


科目:高中化学 来源: 题型:
| A、苯中的甲苯(溴水) |
| B、乙醇中的水(新制CaO) |
| C、甲烷中的乙烯(溴水) |
| D、乙酸乙酯中的乙酸(饱和Na2CO3溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaUH溶液 |
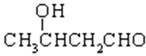

 为主要原料合成
为主要原料合成 ,请设计四步合成路线(无机试剂及溶剂任选).
,请设计四步合成路线(无机试剂及溶剂任选).| O2 |
| 催化剂 |
| CH3CH2OH |
| 浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、t4时刻是增大容器的体积 |
| B、B的起始浓度为0.06mol/L |
| C、t1、t3、t6时刻相比,A物质的量最大的是t6时刻 |
| D、该可逆反应的方程式为:3A(g)?B(g)+2C(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、天然油脂是高分子化合物,同时也是混合物 |
| B、淀粉、纤维素的分子式都是(C6H10O5)n,二者互为同分异构体 |
| C、氨基酸和蛋白质分子中都含有氨基和羧基,二者均有两性 |
| D、糖类、油脂、蛋白质均能发生水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、该蓄电池放电工作时SO42-向正极移动 |
| B、充电时阳极的电极反应式是Pb+SO42--2e-═PbSO4 |
| C、用铅蓄电池电解氯化钠溶液,当阳极上收集到11.2L氯气时(标况下),理论上负极板的质量增加48g |
| D、铅蓄电池为电解电源,当蓄电池中有0.4mol H+被消耗时,电路中通过的电子的物质的量为0.4mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com