
| A. | 4 mol A+2 mol B | B. | 3 mol C+1 mol D+2mol A+1 mol B | ||
| C. | 3mol C+1 mol D+1 mol B | D. | 3 mol C+1 mol D |
分析 A.等效为在原平衡的基础上压强增大一倍到达的平衡状态,与原平衡相比平衡向逆反应方向移动;
B.等效为开始加入4molA+2molB,进一步等效为在原平衡的基础上压强增大一倍到达的平衡状态,与原平衡相比平衡向逆反应方向移动;
C.等效为开始加入2molA+2molB,相当于在原平衡的基础上在加入1molB,与原平衡相比平衡向正反应方向移动;
D.等效为开始加入2molA+1molB,与原平衡为完全等效平衡.
解答 解:A.等效为在原平衡的基础上压强增大一倍到达的平衡状态,与原平衡相比平衡向逆反应方向移动,C的物质的量减小大于混合气体总物质的量减小,故C的物质的量百分含量降低,故A错误;
B.等效为开始加入4molA+2molB,进一步等效为在原平衡的基础上压强增大一倍到达的平衡状态,与原平衡相比平衡向逆反应方向移动,C的物质的量减小大于混合气体总物质的量减小,故C的物质的量百分含量降低,故B错误;
C.等效为开始加入2molA+2molB,相当于在原平衡的基础上在加入1molB,平衡向正反应方向移动,故C的物质的量百分含量增大,故C错误;
D.等效为开始加入2molA+1molB,与原平衡为完全等效平衡,C的物质的量百分含量不变等于w,故D正确,
故选D.
点评 本题考查等效平衡、化学平衡影响因素等,难度中等,构建平衡建立的途径是解题关键.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案科目:高中化学 来源: 题型:解答题
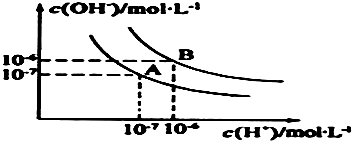 水的电离平衡曲线如图所示:
水的电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子中碳碳键为单双键交替结构 | |
| B. | 苯中含有碳碳双键,所以苯属于烯烃 | |
| C. | 苯与氢气在一定条件下反应生成环己烷 | |
| D. | 苯可以与溴水反应而使其褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅①和④ | B. | 仅①和③ | C. | 仅②和③ | D. | 仅②和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在相同条件下,燃烧等物质的量的C2H4和乙醇,消耗O2体积不相同 | |
| B. | 分子式为C7H8O且属于酚类物质的同分异构体有4种 | |
| C. | 室温下,在水中的溶解度:乙醇>苯酚>乙酸乙酯 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B2)=0.8 mol/(L•s) | B. | v(A2)=0.5 mol/(L•s) | C. | v(C)=0.9 mol/(L•s) | D. | v(B2)=1.2 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
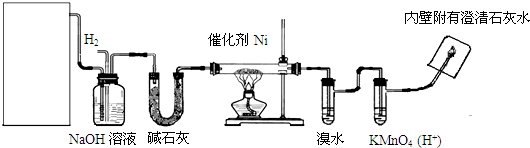
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com