
����Ŀ����84������Һ(��ҵ����Cl2��NaOH��Ӧ�Ƶã�������������Ư�ף�����ʵ������ķ�������ȷ����
ʵ����� |
|
|
|
ʵ������ | ��Ϻ���Һ��pH=9.9,��ʱ����δ��ɫ��һ��ʱ�����ɫ��ȥ�� | ��Ϻ���ҺpH=5.0����ɫѸ����ȥ������������� | ��Ϻ���ҺpH=3.2����ɫѸ����ȥ���������������壬ʹʪ��ĵ��۵⻯����ֽ������ |
A.�Ա�ʵ����������������ɫѸ����ȥ��ԭ���Ƿ����˷�ӦClO+H+�THClO
B.ʵ�����в�����������Cl2����HClO�ֽ�õ���2HClO�TCl2��+H2O
C.�Ա�ʵ������������Һ��pH���ܻ�Ӱ��ClO�������Ի�Cl�Ļ�ԭ��
D.������������84������Һ��Ư��Ч��������Ҫ���غ��ʵ�pH���ܰ�ȫʹ��
���𰸡�B
��������
A. ��84������Һ(��Ч�ɷ�ΪNaClO)��Һ�д����������ˮ����Һ�Լ��ԣ�ˮ�����ɵĴ��������Ư���ԣ���������ٽ�ˮ��ƽ��������У����ɴ�����Ũ�ȴ�Ư��Ч���죬������ɫѸ����ȥ��ԭ���Ƿ����˷�ӦClO+H+�THClO����A��ȷ��
B. ��84������Һ(��Ч�ɷ�ΪNaClO)��Һ�м���Ũ�Ƚϴ��ϡ���ᷴӦ����Ϻ���ҺpH=3.2����ɫѸ����ȥ���������������壬ʹʪ��ĵ��۵⻯����ֽ������˵���������������������Ӻʹ����������������Һ�з���������ԭ��Ӧ������������������ˮ��Ӧ���ɵĴ��������Ư���ԣ����ɵ���������ԣ���B����
C. �Ա�ʵ��ںۣ͢�����ҺŨ�ȴ�С��Ӱ�췴Ӧ���̣���Һ��pH���ܻ�Ӱ��ClO�������Ի�Cl�Ļ�ԭ�ԣ���C��ȷ��
D. ������������84������Һ��Ư��Ч���������Ũ�ȴ�ʱ��������Ⱦ������������Ҫ���غ��ʵ�pH���ܰ�ȫʹ�ã���D��ȷ��
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
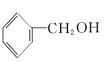
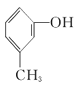
����Ŀ��������5���л���
��![]() ��
�� ��
��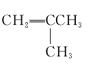 ��
�� ��
��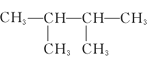
��ش���������:
(1)���л�Ϊͬϵ�����____________��____________����Ϊͬ���칹�����____________��____________(����Żش�)��
(2)��ϵͳ����������������������Ϊ____________��
(3)�л���ں˴Ź�����������____________���塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����õ���Aģ�ҵ���Ʊ�������D�Ĺ�����ͼ��ʾ����֪DΪǿ�ᣬ��ش��������⡣
![]()
(1)��A�ڳ�����Ϊ���壬B����ʹƷ����Һ��ɫ���д̼�����ζ����ɫ���塣
��D�Ļ�ѧʽ��________��
���ڹ�ҵ�����У�B����Ĵ����ŷű���ˮ���պ��γ���____________����Ⱦ�˻�����
(2)��A�ڳ�����Ϊ���壬C�Ǻ���ɫ�����塣
��A�Ļ�ѧʽ��____________��C�Ļ�ѧʽ��____________��
��D��Ũ��Һ�ڳ����¿���ͭ��Ӧ������C���壬��Ӧ�Ļ�ѧ����ʽ��_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ϵķ��������̷�Ϊԭ�ϣ������������ա���Ӧ�Ļ�ѧ����ʽΪ��2FeSO4��7H2O![]() Fe2O3+ SO2��+ SO3��+ 14H2O����������������ˮ����ͬʱ������õ����ᡣ����ͼװ��ģ�����̷��������ʵ�飬���������ɵ�����Ͷ���������װ������ȥ��������bΪ������Թܡ����й��ڸ÷�Ӧ˵����ȷ����
Fe2O3+ SO2��+ SO3��+ 14H2O����������������ˮ����ͬʱ������õ����ᡣ����ͼװ��ģ�����̷��������ʵ�飬���������ɵ�����Ͷ���������װ������ȥ��������bΪ������Թܡ����й��ڸ÷�Ӧ˵����ȷ����
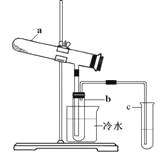
A.������Ӧ�����������ͨ��BaCl2��Һ�У������ij���ΪBaSO3��BaSO4
B.b�в�������ɫʯ����Һ���ɼ��������H+��SO42��
C.Ϊ���鷴Ӧ����һ��������Թ�c��Ӧ������Լ�ΪNaOH��Һ
D.b�����õ����������������Ϊ29.5%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����û�ѧ��Ӧԭ���о�̼��������ĵ��ʼ��仯����ķ�Ӧ�Ի������Ⱦ����ԴΣ��������Ҫ���塣
I.��Ϊ��Ҫ�Ļ���ԭ�ϣ��й㷺��;��
��1���ϳɰ��е������������з�Ӧ��ȡ��
a. CH4(g)+H2O(g)CO(g)+3H2(g) H1=+216.4kJ/mol
b. CO(g)+H2O(g)CO2(g)+H2(g) H2=-41.2kJ/mol
��ӦCH4(g)+2H2O(g)CO2(g)+4H2(g) H=___��
��2����ʼʱͶ�뵪�������������ʵ����ֱ�Ϊ1mol��3mol���ڲ�ͬ�¶Ⱥ�ѹǿ�ºϳɰ���ƽ��ʱ������а�������������¶ȵĹ�ϵ��ͼ��
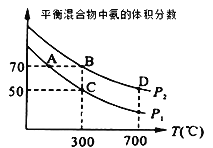
�ٺ�ѹʱ����Ӧһ���ﵽƽ��״̬�ı�־��___(�����)
A. N2��H2��ת������� B. ��Ӧ��ϵ�ܶȱ��ֲ���
C. ![]() ���ֲ��� D.
���ֲ��� D. ![]() =2
=2
��P1___P2 (����>����=������<������ͬ)����Ӧ��ƽ�ⳣ����B��___D�㡣
��C��H2��ת����Ϊ__��
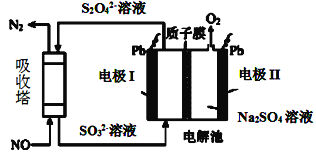
��.�ü�ӵ绯ѧ��ȥ��������NO��ԭ����ͼ��ʾ��
��3����֪��������Һ�����ԣ��������ĵ缫��ӦʽΪ____����Ӧ������ͨ������Ĥ��H+Ϊ2molʱ�������������ɵ������ڱ�״���µ����Ϊ____L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з����е�����ԭ���ӻ������������ͬ����(����)
A.CO2��SO2B.CH4��NH3
C.BeCl2��BF3D.C2H4��C2H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����O2��HClת��ΪCl2�������Ч�棬������Ⱦ��
��1����ͳ�ϸ�ת��ͨ����ͼ��ʾ�Ĵ���ѭ��ʵ�֣�
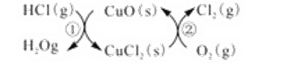
���У���Ӧ��Ϊ��2HCl��g�� + CuO��s��![]() H2O��g��+CuCl2��g�� ��H1
H2O��g��+CuCl2��g�� ��H1
��Ӧ������1molCl2��g���ķ�Ӧ��Ϊ��H2�����ܷ�Ӧ���Ȼ�ѧ����ʽΪ___________����Ӧ������H1����H2��ʾ����
��2������RuO2����������HClת��ΪCl2���ܷ�Ӧ���и��õĴ����ԣ�
��ʵ������һ��ѹǿ�£��ܷ�Ӧ��HClƽ��ת�������¶ȱ仯��aHCl��T������ͼ�����ܷ�Ӧ����H___0������������������������������A��B�����ƽ�ⳣ��K��A����K��B���нϴ����_______��
��������ʵ������ѹ�����ʹѹǿ��������ӦaHCl��T���ߵ�ʾ��ͼ������Ҫ˵������______________��
�����д�ʩ�����������aHCl����___________��
A������n��HCl�� B������n��O2��
C��ʹ�ø��õĴ��� D����ȥH2O
��3��һ�������²�÷�Ӧ������n��Cl2�����������£�
t��min�� | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
n��Cl2��/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
����2.0��6.0min����HCl�����ʵ����仯��ʾ�ķ�Ӧ����______����mol��min-1Ϊ��λ��д��������̣���
��4��Cl2��;�㷺��д����Cl2�Ʊ�Ư�۵Ļ�ѧ����ʽ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CaSO4����O2��ȼ��CO��Ӧ��һ�ָ�Ч����������ȼ�ռ������������·�Ӧ��
��![]() CaSO4(s)��CO(g)
CaSO4(s)��CO(g) ![]() CaS(s)��CO2(g)����H1����47.3 kJ��mol��1
CaS(s)��CO2(g)����H1����47.3 kJ��mol��1
��CaSO4(s)��CO(g) CaO(s)��CO2(g)��SO2(g) ��H2����210.5 kJ��mol��1
��CO(g) ![]() C(s)��
C(s)��![]() CO2(g)����H3����86.2 kJ��mol��1
CO2(g)����H3����86.2 kJ��mol��1
����˵���������� (�� ��)
A. ��Ӧ�ٴﵽƽ��ʱ������ѹǿƽ�ⲻ�ƶ�
B. ��Ӧ�ڵ�ƽ�ⳣ������ʽΪK��![]()
C. ��Ӧ�ٺ͢�������Ӧ����Ӧ���Ǹ���Ӧ
D. 2CaSO4(s)��7CO(g) ![]() CaS(s)��CaO(s)��6CO2(g)��C(s)��SO2(g)�Ƿ��ȷ�Ӧ
CaS(s)��CaO(s)��6CO2(g)��C(s)��SO2(g)�Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ѿ��ﵽ��ѧƽ��Ŀ��淴Ӧ4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g)�������������䣬���ݼ�Сѹǿ������������ȷ���� �� ��
4NO(g) + 6H2O(g)�������������䣬���ݼ�Сѹǿ������������ȷ���� �� ��
A.ƽ��������Ӧ�����ƶ�������Ӧ���������淴Ӧ���ʼ�С
B.ƽ��������Ӧ�����ƶ���Kֵ����
C.�����ʵ�Ũ�ȶ���С����������ʵ�������
D.�����淴Ӧ���ʶ���С�����淴Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com