
��ͼ������A��M��һ�������µ�ת����ϵ�����ֲ��P��Ӧ����δ�г��������У�I���ɵ�������Ԫ����ɵĵ������۵���ߵĽ����� K��һ�ֺ���ɫ���塣
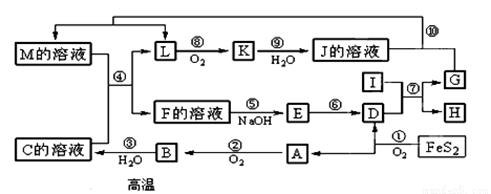
����д���пհף�
��1�������ڱ��У���ɵ���G��Ԫ��λ�ڵ�____________����_________�塣
��2�� �ڷ�Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ___________________��
��3���ڢڡ��ۡ��ޡ����м����ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ����___________������ţ�
��4�� ��Ӧ�ܵ����ӷ���ʽ�ǣ�__________________________________��
��5�� ��������D��KNO3��KOH���ڣ����Ƶ�һ�֡���ɫ��������Ч��ˮ��K2FeO4��������أ��� ͬʱ������KNO2��H2O���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�
_________________________ ��
 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ����ʮУ���н̸Ĺ�ͬ��߶�����ĩ��ѧ�Ծ��������棩 ���ͣ������
������̼�IJ����������ҹ���Դ�����һ����Ҫս�Է���
��1���û���̿��ԭ�����Դ�������β���еĵ������ij�о�С����ij�ܱ���������һ�����Ļ���̿��NO��������ӦC(s) + 2NO(g)  N2(g) + CO2(g) ��H,��T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ���Ũ�����£�
N2(g) + CO2(g) ��H,��T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ���Ũ�����£�
ʱ��/min Ũ��/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.96 | 0.96 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
CO2 | 0 | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
�ٸ���ͼ�����ݷ���T1��ʱ���÷�Ӧ��0-20min��ƽ����Ӧ����
v(N2)= mol��L��1��min��1������÷�Ӧ��ƽ�ⳣ��K= ��
��30min��ֻ�ı�ijһ�����������ϱ��������жϸı������������ (����ĸ����)��
A��������ʵĴ���
B���ʵ���С���������
C��ͨ��һ������NO
D������һ�����Ļ���̿
����30min�������¶���T2�棬�ﵽƽ��ʱ��������NO��N2��CO2��Ũ��֮��Ϊ5:3:3����ﵽ��ƽ��ʱNO��ת���� (����ߡ����͡�)����H 0(�>����<��).
��2����ҵ����CO2��H2��Ӧ�ϳɶ����ѡ���֪��
CO2(g)��3H2(g) CH3OH(g)��H2O(g) ��H1����49.1 kJ��mol��1
CH3OH(g)��H2O(g) ��H1����49.1 kJ��mol��1
2CH3OH(g) CH3OCH3(g)��H2O(g) ��H2����24.5 kJ��mol��1
CH3OCH3(g)��H2O(g) ��H2����24.5 kJ��mol��1
д��CO2(g)��H2(g)ת��ΪCH3OCH3(g)��H2O(g)���Ȼ�ѧ����ʽ ��
��3��������ȼ�ϵ�ؾ�������ת���ʸߡ���������ص�����㷺Ӧ�ã�һ�ֶ������������(�����ΪKOH��Һ)�ĸ�����ӦʽΪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
������Ȼ�����ѽ���ȡ��Ȳ��������������Ϊ�����о����ȵ㣬��������Ҫ��ӦΪ��2CH4(g) C2H2(g)+3H2(g) ��H=a kJ•mol-1������Ӧ��2CH4(g)
C2H2(g)+3H2(g) ��H=a kJ•mol-1������Ӧ��2CH4(g) C2H4(g)+2H2(g) �ش��������⣺
C2H4(g)+2H2(g) �ش��������⣺
��1����Ȼ�����ѽ����ʹ�õĴ����к���SiO2��Al2O3�ȶ����ѱ���ԭ�������д��SiO2������������;��_______________________��д��Al2O3����Լ���Һ��Ӧ�����ӷ���ʽ___________________��
��2����֪�����ȼ���ȡ�H=-890.3kJ•mol-1����Ȳ��ȼ���ȡ�H=-1299.6kJ•mol-1��������ȼ���ȡ�H=-285.8kJ•mol-1������ʽ�е�a=___________��
��3����Ȼ��������������������������������ͼ��ʾ��ȼ�ϵ���зŵ�(������Li2CO3��K2CO3Ϊ�����)��д��ȼ�ϼ��Ϸ����ĵ缫��Ӧʽ_______________________________��

��4��ij�¶��£���1L�����ܱ������г���0.3mol���飬��������ʹ��ֻ������������Ӧ���ﵽƽ��ʱ�����c(C2H4)=c(CH4)����������¼����ƽ��ת����Ϊ__________��
��5����Ȼ���ѽ�����У�ƽ��ʱ�������ѹ(��λΪPa)�Ķ���(��)���¶�(T)֮��Ĺ�ϵ����ͼ��

�ٸ���Ӧ2CH4(g) C2H4(g)+2H2(g) �ġ�H__________(���������)0��
C2H4(g)+2H2(g) �ġ�H__________(���������)0��
������ͼ�����ݼ���A���¶�����Ҫ��Ӧ2CH4(g) C2H2(g)+3H2(g)��ƽ�ⳣ��__________(����ƽ���ѹ����ƽ��Ũ�ȼ��㣬
C2H2(g)+3H2(g)��ƽ�ⳣ��__________(����ƽ���ѹ����ƽ��Ũ�ȼ��㣬 )��
)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��ij�㶨�¶��£����ݻ�Ϊ1L��������Ͷ��1mol CO��2mol H2O���������·�Ӧ��
CO(g)+H2O(g) CO2(g)+H2(g)��ƽ��ʱ����CO2 2/3mol���������¶Ⱥ��ݻ����䣬����������2mol H2O(g)��ʹ��Ӧ�����µ�ƽ�⣬����˵������ȷ����
CO2(g)+H2(g)��ƽ��ʱ����CO2 2/3mol���������¶Ⱥ��ݻ����䣬����������2mol H2O(g)��ʹ��Ӧ�����µ�ƽ�⣬����˵������ȷ����
A���¡���ƽ��ʱ�����������ѹǿ֮����5��3
B����ƽ��ʱH2O��ת����Ϊ20%
C����ƽ��ʱCO��Ũ����0.2 mol•L��1
D���¡���ƽ��ʱ�����������ܶ�֮��Ϊ5��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���ܱ������������з�Ӧ��aA(g) cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����
cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����
A��ƽ��������Ӧ�����ƶ�
B��a��c��d
C��D�������������
D��A��ת���ʱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�������У���ij��̼ԭ������4����ͬ��ԭ�ӻ�ԭ���ţ�������̼ԭ�ӳ�Ϊ������̼ԭ�ӡ�������һ������̼ԭ�ӵ�����һ�����й�ѧ���ԡ����ʣ� �й�ѧ���ԣ����������з�Ӧ�����ɵ��л�����ѧ���Ե��ǣ��� ��
�й�ѧ���ԣ����������з�Ӧ�����ɵ��л�����ѧ���Ե��ǣ��� ��
A. ��NaOH��Һ����
B. ����ᷢ��������Ӧ
C. ��������Һ����������Ӧ
D. �ڴ�����������H2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
0.1mol/L������Һ 100mL�У�����0.1mol/L�� Ba��OH��2��Һ����SO42-ǡ�ó�����ȫʱ��ͬʱ�õ����������������ʵ���Ϊ�� ��
A��0.01mol B��0.005mol C��0.0133mol D��0.0mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ��ɽ�и�һ����ĩ�Ŀƻ�ѧ�Ծ��������棩 ���ͣ������
�Ҵ��������������г����������л���Իش��������⣺
��1���Ҵ��й����ŵ�������__________�������й����ŵĽṹ��ʽΪ____________
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��
�� �Ҵ�ȼ�� _____________________________________________________
�� �Ҵ���Na _____________________________________________________
�� ������NaHCO3_____________________________________________________
�� ������CH3OH______________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�����и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ʵ����
�Ե���Ϊ��Ҫԭ�Ϻϳ�һ�־��й���ζ������C�ͻ�����D�ĺϳ�·����ͼ��ʾ��
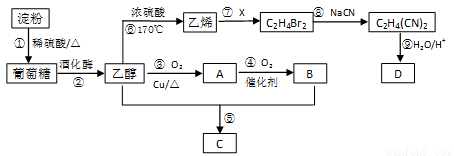
��ش��������⣺
��1��A�Ľṹ��ʽΪ ��B�����еĹ���������Ϊ ��
��2����Ӧ��������X�ķ���ʽΪ ����Ӧ�������Ϊ ��
��3����Ӧ�ݵĻ�ѧ����ʽΪ ��
��Ӧ������ʵ��������ϩ��Ϊ��ȥ���п��ܻ��е�SO2Ӧѡ�õ��Լ��� ��
��4����֪D����Է�����Ϊ118������̼������Ԫ�ص����������ֱ�Ϊ40.68%��5.08%������Ϊ��Ԫ�أ���D�ķ���ʽΪ ��
��5���벹������֤����Ӧ���Ƿ�Ӧ��ȫ��ʵ�鷽���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com