
����Ŀ���ڢ١��ڡ����ݻ����ȵĺ����ܱ������У�������0.1molCO��0.2molH2���ڴ����������·�����Ӧ��CO(g)+2H2(g)![]() CH3OH(g)���������������ƽ��������CH3OH������������¶ȵı仯��ͼ��ʾ������˵����ȷ���ǣ� ��
CH3OH(g)���������������ƽ��������CH3OH������������¶ȵı仯��ͼ��ʾ������˵����ȷ���ǣ� ��
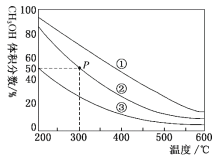
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ
B.���������ݻ�����>��>��
C.��P�㣬COת����Ϊ75%
D.��P�㣬�����������ٳ���CO��H2��CH3OH��0.025mol����ʱv(CO)��>v(CO)��
���𰸡�CD
��������
A��ͬһ�����У������¶ȣ��״������������С��˵�������¶�ƽ�������ƶ���������Ӧ�Ƿ��ȷ�Ӧ����A����
B����ͬ�¶��£�����ѹǿ(��С�����ݻ�)ƽ�������ƶ�����״����������������ͼ֪����ͬ�¶��¼״������������С˳���ǣ��٣��ڣ��ۣ�˵��ѹǿ��С˳���ǣ��٣��ڣ��ۣ����������Ϊ���٣��ڣ��ۣ���B����
C��P�㣬�����м״������������50%�����ʱCO��ת����Ϊx��������ʽ��
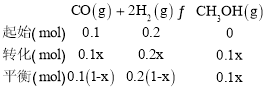
ͬһ���������������������������ʵ�������������![]() =50%�����x=0.75��CO��ת����Ϊ75%����C��ȷ��
=50%�����x=0.75��CO��ת����Ϊ75%����C��ȷ��
D�����������ΪVL��P�㻯ѧƽ�ⳣ��K=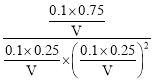 =1200V2�������������ٳ���CO��H2��CH3OH��0.025mol����ʱŨ����=
=1200V2�������������ٳ���CO��H2��CH3OH��0.025mol����ʱŨ����=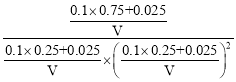 =355.5V2��K����ƽ�������ƶ������Դ�ʱv(CO)����v(CO)������D��ȷ��
=355.5V2��K����ƽ�������ƶ������Դ�ʱv(CO)����v(CO)������D��ȷ��
�ʴ�ΪCD��


 Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д� ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�صĻ���������࣬����Ҳ������ͬ����ش��������⣺
��1��NO2�н�ǿ�������ԣ��ܽ�SO2������SO3����������ԭΪNO����֪��������Ӧ�����������仯��ͼ1��ͼ2��ʾ����NO2����SO2����SO3(g)���Ȼ�ѧ����ʽΪ____��
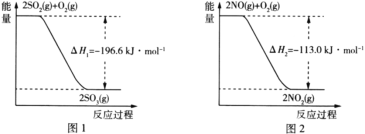
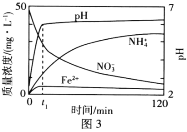
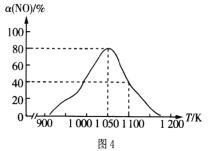
��2���ڵ��������£���ʵ��������������Fe�ۻ�ԭKNO3��Һ��pH =2.5������Ӧ��������Һ��������ӵ�����Ũ�ȡ�pH��ʱ��ı仯���ߣ����ָ���Ӧ����������ȥ����ͼ3��ʾ�������ͼ3����Ϣд��![]() minǰ��Ӧ�����ӷ���ʽ____��
minǰ��Ӧ�����ӷ���ʽ____��
��3���о���Ա�û���̿������β���е�NO����������������ӦC(s) +2NO(g)![]() N2(g) +CO2(g)
N2(g) +CO2(g) ![]() H<0���ں�ѹ�ܱ������м��������Ļ���̿��һ������NO���壬��Ӧ��ͬʱ��ʱ�����NO��ת����
H<0���ں�ѹ�ܱ������м��������Ļ���̿��һ������NO���壬��Ӧ��ͬʱ��ʱ�����NO��ת����![]() (NO)���¶ȵı仯��ͼ4��ʾ��
(NO)���¶ȵı仯��ͼ4��ʾ��
����ͼ4��֪���¶ȵ���1 050 Kʱ��NO��ת�������¶����߶�����ԭ����__���¶�Ϊ1050 KʱCO2��ƽ���������Ϊ__��
�����ڷ�ӦC(s) +2NO(g)![]() N2(g)+CO2(g)�ķ�Ӧ��ϵ����ƽ�ⳣ��
N2(g)+CO2(g)�ķ�Ӧ��ϵ����ƽ�ⳣ��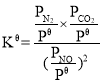 ������
������![]() Ϊ��ѹǿ��1��105Pa����
Ϊ��ѹǿ��1��105Pa����![]() ��
��![]() ��
��![]() Ϊ����ֵ�ƽ���ѹ����
Ϊ����ֵ�ƽ���ѹ����![]() =
=![]() ��
��![]() ��
��![]() Ϊƽ����ѹ��
Ϊƽ����ѹ��![]() Ϊƽ��ϵͳ�� NO�����ʵ�����������NO����ʼ���ʵ���Ϊ1 mol�����跴Ӧ�ں㶨�¶Ⱥͱ�ѹǿ�½��У�NO��ƽ��ת����Ϊ
Ϊƽ��ϵͳ�� NO�����ʵ�����������NO����ʼ���ʵ���Ϊ1 mol�����跴Ӧ�ں㶨�¶Ⱥͱ�ѹǿ�½��У�NO��ƽ��ת����Ϊ![]() ����
����![]() =__���ú�
=__���ú�![]() �����ʽ��ʾ����
�����ʽ��ʾ����
��4�������ִ��ֳּ���������̽��ѹǿ��2NO2 (g)![]() N2O4(g)ƽ���ƶ���Ӱ�졣�ں㶨�¶Ⱥͱ�ѹǿ�����£�����Ͳ�г���һ�������NO2������ܷⲢ���ֻ���λ�ò��䡣�ֱ���
N2O4(g)ƽ���ƶ���Ӱ�졣�ں㶨�¶Ⱥͱ�ѹǿ�����£�����Ͳ�г���һ�������NO2������ܷⲢ���ֻ���λ�ò��䡣�ֱ���![]() s��
s��![]() sʱѸ���ƶ��������ֻ���λ�ò��䣬�ⶨ��Ͳ������ѹǿ�仯��ͼ5��ʾ��
sʱѸ���ƶ��������ֻ���λ�ò��䣬�ⶨ��Ͳ������ѹǿ�仯��ͼ5��ʾ��
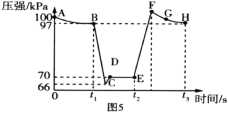
��B��E�����Ӧ������Ӧ���ʴ�СΪ![]() __������ > ���� < ������ =����
__������ > ���� < ������ =����![]() ��
��
��E��F��G��H�ĵ��Ӧ�����ƽ����Է����������ĵ�Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�������ʵ�鷽�����Է���KCl��BaCl2���ֹ�������Իش��������⣺

��ѡ�Լ���Na2SO4��Һ��K2CO3��Һ��K2SO4��Һ������
(1)�����ٵ�������________�������ڵ�������____________��
(2)�Լ�a��____________(�ѧʽ����ͬ)���Լ�b��__________,����B��____________��
(3)�����Լ�a��������Ӧ�Ļ�ѧ����ʽΪ__________________________________��
�����Լ�b��������Ӧ�Ļ�ѧ����ʽΪ____________________________________��
(4)�÷����ܷ�ﵽʵ��Ŀ�ģ�__________________________(��ܡ����ܡ�)�������ܣ�Ӧ��θĽ���(���ܣ����ʲ��ûش�)__________��
(5)��Ҫ�ⶨԭ�������BaCl2����������������Ҫȷ���������������⣬���ٻ�Ҫ��õ�������____��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.�ҹ����ຣʡ�������κ�ʢ��ʳ�Σ�������ʳ�ι�ϵ���У�ʳ�����ϰ���������ִ����Ĺ�ũҵ�����о�����Ҫ���á������к�Ca2����Mg2����SO42���Լ���ɳ�����ʣ�Ϊ�˳�ȥ���������ʣ�������ʵ�鲽������ᴿ��
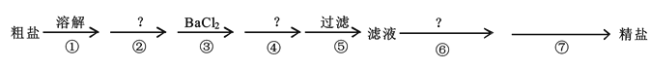
��1���ܲ������Լ���____��
��2���ڢ�������Ӧ�����ӷ���ʽΪ____��____��
��3���ڢ߲��IJ�������____����Ҫ�IJ���������____��____��
��4��ͨ��������й��˺����Һ������SO42���ѳ����IJ���������____��
��.��1���谢���ӵ�����ΪNA����״���£�ijO2��N2�Ļ������m g����b�����ӣ���n g�û����������ͬ״������ռ�������____L��
��2����xR2��+yH��+O2�TmR3��+nH2O�����ӷ���ʽ�У��Ի�ѧ������m��R2����R3���ж���ȷ����____��
A��m=y��R3������������ B��m=2y��R2��������
C��m=2��R3���������� D��m=4��R2���ǻ�ԭ��
��3����˫���ŷ�������з�Ӧ�ĵ���ת�Ʒ������Ŀ____��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.�����£���ӦNH3(g)+HCl(g)=NH4Cl(s)���Է�������Ӧ����÷�Ӧ�ġ�H>0
B.�����£������ʵ���Ũ�ȵ�CH3COOH��Һ��HCl��Һ�У�ˮ�ĵ���̶���ͬ
C.�����£�0.1molL��1CH3COONa��Һ��ˮϡ�ͺ���Һ��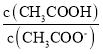 ��ֵ����
��ֵ����
D.�����£���BaCO3��BaSO4�ı�����Һ�м�������BaCl2���壬��Һ��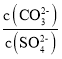 ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�wgij���������������г��ȼ�գ���ȼ�ղ��������������Na2O2��Ӧ��������������wg������H2����CO����CO��H2�Ļ���� ����ȩ��HCHO������CH3COOH���������ǣ�C6H12O6���У������������ ( )
A.��������B.ֻ���٢ڢ�C.ֻ���ܢ�D.ȫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��120mL����0.20mol̼���Ƶ���Һ��200mL���ᣬ���ܽ�ǰ�ߵ�����ߣ����ǽ����ߵ���ǰ�ߣ�����������������������ɵ����������ͬ���ұ�ֵΪ5��2���������Ũ���ǣ���������
A.2.0mol/LB.1.0mol/LC.0.18mol/LD.1.25mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���һЩ������ȼ���ȣ������б�����ȷ����
������ | ȼ����/ kJ��mol-1 | ������ | ȼ����/ kJ��mol-1 |
���� | 891.0 | ������ | 2878.0 |
���� | 1560.8 | �춡�� | 2869.6 |
���� | 2221.5 | ������ | 3531.3 |
A. �������ȼ���ȴ���3531.3 kJ��mol-1
B. ��ͬ������������̼����������Խ��ȼ�շų�������Խ��
C. ������ת��Ϊ�춡����Ȼ�ѧ����ʽΪ��CH3CH2CH2CH3(g) ![]() CH3CH(CH3)CH3(g) ��H =+8.4kJ��mol-1
CH3CH(CH3)CH3(g) ��H =+8.4kJ��mol-1
D. ����ȼ�յ��Ȼ�ѧ����ʽΪ��CH4(g)+2O2(g) ![]() CO2(g) +2H2O(g) ��H =-891.0kJ��mol-1
CO2(g) +2H2O(g) ��H =-891.0kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.Na2O2����ʪ�����ɫʯ����ֽ��ʯ����ֽ���ձ����ɫ
B.Na2O2�����������Ӻ������Ӹ�����Ϊ2:1
C.Na2O2��CO2��Ӧ����0.1 mol O2ʱת�Ƶ���0.4 mol
D.���ռ���Һ�м���2 g Na2O2����ַ�Ӧ�����Һ��c(Na��)����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com