
【题目】下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是( )
A.6与16B.11与17C.14与8D.10与19
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔(C2H2).
(1)CaC2中C22﹣与O22+互为等电子体,O22+的电子式可表示为;1mol O22+中含有的π键数目为 .
(2)乙炔与氢氰酸反应可得丙烯腈(H2C=CH﹣C≡N).丙烯腈分子中碳原子轨道杂化类型是;分子中处于同一直线上的原子数目最多为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多氯代甲烷常为有机溶剂,其中分子结构为正四面体的是 . 工业上分离这些多氯代物的方法是 .
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式(不考虑立体异构).
(3)聚氯乙烯是生活中常用的塑料.工业生产聚氯乙烯的一种工艺路线如下: ![]()
反应①的化学方程式为 , 反应类型为;反应②的反应类型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应: 2A(g)+B(g) ![]() 2C(g),若经2s(秒)后测得C的浓度为0.6mol·L-1现有下列几种说法:
2C(g),若经2s(秒)后测得C的浓度为0.6mol·L-1现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol·L-1·S-1②用物质B表示的反应的平均速率为0.6mol·L-1·S-1③2s时物质A的转化率为70%④2s时物质B的浓度为0.7mol·L-1
其中正确的是( )
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
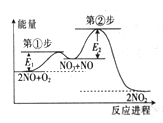
【题目】反应2NO(g)+O2(g)=2NO2(g)由①、②两步反应构成,其反应进程与能量关系如图,所示。已知:
①NO+O2 =NO3(快反应);②NO3+NO=2NO2(慢反应)。下列说法正确的是
A. NO3比NO稳定
B. ①、②两步反应均为放热反应
C. 第②步的逆反应的活化能更大,因此NO2更容易转化为NO3和NO
D. 升高温度,①、②两步反应速率均加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关多电子原子的叙述中正确的是( )
A. 在一个多电子原子中,不可能有两个运动状态完全相同的电子
B. 在一个多电子原子中,不可能有两个能量相同的电子
C. 在一个多电子原子中,N层上的电子能量肯定比M层上的电子能量高
D. 某个多电子原子的3p能级上仅有两个电子,它们的自旋状态必然相反
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.ΔH<0,ΔS>0的反应在温度低时不能自发进行
B.在其他条件不变时,增大反应物的浓度,可以增大活化分子百分数
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D.NH4HCO3(g)===NH3(g) +H2O(g)+CO2(g) ΔH =+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物质资源是一种污染小的可再生能源。生物质的主要转化途径及主要产物如下图。

(1)下列有关说法正确的是_____________。
a.生物质能,本质上能量来源于太阳能
b.由纤维素水解获得的乙醇作燃料是利用了生物质能
c.生物质裂解获得的汽油、柴油等属于纯净物
d.由植物秸杆等厌氧发酵获得的沼气,主要成分是甲烷
(2)由生物质能获得的CO和H2,可以合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者1∶1催化反应,其原子利用率达100%,合成的物质可能是____________。
a.汽油 b.甲醇(CH3OH) c.甲醛(HCHO) d.乙酸(CH3COOH)
(3)甲醇是一种重要的化工原料,工业上合成甲醇的反应:CO(g)+2H2(g) ![]() CH3OH(g) △H=﹣90.8kJ·mol-1。若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
CH3OH(g) △H=﹣90.8kJ·mol-1。若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molCO 、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
CH3OH的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
平衡常数 | K1 | K2 | K3 |
反应物转化率 | α 1 | α 2 | α 3 |

下列说法正确的是________________。
a.c1 = c2 b.2Q1 = Q3 c.K1 = K3 d.α2 + α3<100%
(4)某实验小组设计如图b所示的电池装置,正极的电极反应式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com