
分析 (1)S+2KNO3+3C═K2S+N2↑+3CO2↑中,S、N元素的化合价降低,C元素的化合价升高;
(2)乙烯能用作水果催熟剂,只有蔗糖可水解,只有乙酸具有酸性.
解答 解:(1)S+2KNO3+3C═K2S+N2↑+3CO2↑中,S、N元素的化合价降低,C元素的化合价升高,则KNO3为氧化剂,得到电子被还原,C为还原剂,
故答案为:被还原;还原剂;
(2)有机物①CH2=CH2、②CH3COOH、③蔗糖、④苯中,能用作水果催熟剂的是①,能发生水解反应的是③,能使紫色石蕊溶液变红的是②,故答案为:①;③;②.
点评 本题考查氧化还原反应及有机物的性质,为高频考点,把握反应中元素的化合价变化、物质性质为解答的关键,注意有机物的官能团决定性质,题目难度不大.


科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
下列依据相关实验得出的结论正确的是
A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
B.将Fe(NO3)2样品溶于稀盐酸中,然后滴加KSCN溶液,溶液变红,说明Fe(NO3)2样品已氧化变质
C.在食盐试样中加入盐酸和KI溶液,加入淀粉溶液后变蓝,说明食盐试样中可能含有KIO3
D.加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在某些工具的机械转动部位刷油漆以防锈 | |
| B. | 自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 | |
| C. | 自行车车辐条上的镀锌层部分破损,还可以为铁提供保护 | |
| D. | 钢铁在潮湿的环境中更易生锈,要在电线外面包上一层塑料层以防锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
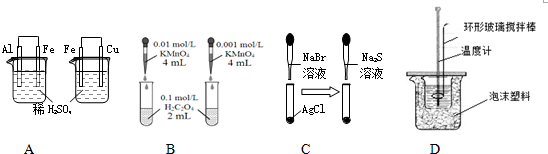
| A. | 依据左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡,判断活动性:Al>Fe>Cu | |
| B. | 依据褪色快慢比较浓度对反应速率的影响 | |
| C. | 依据白色固体先变为淡黄色,后变为黑色(Ag2S),判断溶解性:AgCl>AgBr>Ag2S | |
| D. | 用该装置测定中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-?+H2↑ | |
| B. | 金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-?+H2↑ | |
| C. | 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列说法正确的是( )
一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列说法正确的是( )| A. | 反应开始到t2时,反应达到平衡状态 | |
| B. | 反应开始到t1(t1=1s),N的物质的量浓度变化了2mol/L | |
| C. | 反应开始到t2(t2=2s),用M表示反应速率为0.5mol/(L.s) | |
| D. | 反应的化学方程式为:N(g)?2M(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a b c d | B. | a c d b | C. | c a b d | D. | b d c a |
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第二次模拟化学试卷(解析版) 题型:选择题
用氯气和绿矾处理水,下列说法错误的是( )
A.氯气起杀菌消毒作用
B.氯气氧化绿矾
C.绿矾具有净水作用
D.绿矾的氧化产物具有净水作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com